
【题目】下图为教科书中电解饱和食盐水的实验装置。据此,下列叙述不正确的是
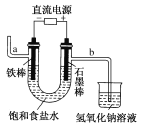
A. 装置中a管能产生氢气
B. b管导出的是氯气
C. 在石墨棒电极区域有NaOH生成
D. 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”
【答案】C
【解析】
根据图知,Fe作阴极、石墨棒作阳极,Fe电极反应式为2H2O+2e―=H2↑+2OH―,石墨棒电极反应式为2Cl――2e―=Cl2↑,则a得到的气体是氢气、b管导出的气体是氯气,Fe棒附近有NaOH生成,据此分析解答。
A.根据图知,Fe作阴极、石墨棒作阳极,Fe电极反应式为2H2O+2e―=H2↑+2OH―,石墨棒电极反应式为2Cl――2e―=Cl2↑,则a得到的气体是氢气、b管导出的气体是氯气,故A正确;
B.根据A知,b管导出的气体是氯气,故B正确;
C.根据A知阴极氢离子放电,破坏水的电离平衡,Fe电极附近有NaOH生成,石墨电极附近没有NaOH生成,故C错误;
D.该电解池电解过程中有氯气、氢气和NaOH生成,所以以食盐水为基础原料制取氯气等产品的工业称为“氯碱工业”,故D正确;
答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有三组实验:①除去混在植物油中的水;②对碘水中的碘进行浓缩;③对30%的酒精溶液中的酒精进行提纯。以上实验采用的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。
Ⅰ.制备苯甲酸和回收未反应的甲苯
反应原理:
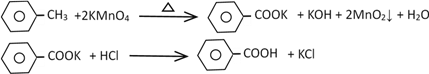
第1步:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应;
第2步:过滤反应混合物,得到滤液;经过操作Ⅰ,得到有机层和水层;
第3步:向有机层中加无水Na2SO4,过滤,经过操作Ⅱ,得到无色液体A;
第4步:向水层加入浓盐酸酸化,蒸发浓缩,冷却,过滤,得到白色固体B;
已知:
相对分子质量 | 熔点 | 沸点 | 密度 | 溶解度 | |
甲苯 | 92 | -95℃ | 110.8℃ | 0.8669g·mL-1 | 极微溶于水 |
苯甲酸 | 122 | 122.4℃ | 249℃ | 1.2659 g·mL-1 | 0.3g (25℃时) 6.9g (95℃时) |
(1)操作Ⅰ所用的玻璃仪器有烧杯和______________,操作Ⅱ为________________。
(2)第3步中加入无水Na2SO4的目的是_____________________,无色液体A是_______。
Ⅱ.提纯粗苯甲酸
该同学利用重结晶的方法对得到的B进行提纯。重结晶的过程:加热溶解→趁热抽滤→冷却结晶→抽滤→洗涤→干燥→纯苯甲酸。(注:抽滤装置如图所示,主要仪器有A布氏漏斗,B抽滤瓶,抽气泵等)
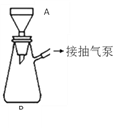
(3)白色固体B中的杂质是____________。
(4)趁热抽滤得到的滤液放置冷却可以结晶出纯净的苯甲酸晶体,为了得到更多的苯甲酸,是不是温度越低越好并说明理由______(填“是”或“不是”),理由__________________________________________________________。
(5)使用抽滤装置比普通过滤装置的优点是_______________________________________。
(6)实验中取甲苯10.0 mL,制得苯甲酸8.0g,本次实验中苯甲酸的产率为____________(结果保留到小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是__________(填物理变化、化学变化);
(2)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为________________________________,其中氧化剂是_______还原剂是________。尾气处理的离子方程式为______________________________。
(3)工业上制备漂白粉的化学方程式___________________________________。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用方程式或化学式回答下列问题:
将氯水滴加紫色石蕊溶液中,先变红后褪色______________________________(化学方程式)其中,变红后褪色是因为有_________(化学式)生成具有漂白性;
将氯水滴入硝酸银溶液中,有白色沉淀生成__________________________。(离子方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
氧化物 | 环境问题 | 主要来源 | |
A | CO2 | 酸雨 | 化石燃料的燃烧 |
B | CO | CO中毒 | 汽车尾气和化石燃料的不完全燃烧 |
C | NO2 | 温室效应 | 工厂废气的排放 |
D | SO2 | 光化学烟雾 | 汽车尾气的排放 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为蒸馏实验装置。
(1)写出下列仪器的名称:a.__________; b.___________;
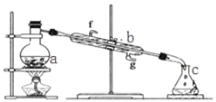
(2)实验过程中,需要通冷水,图中的进水方向是_______进(填图中字母);
(3)若利用装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77℃)的混合物,还缺少的仪器是_______;
II.现用NaOH固体配制0.1 mol/L NaOH溶液480mL,据此回答下列问题:
(4)配制氢氧化钠溶液需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和______;
(5)实验时需要称量氢氧化钠_______g;
(6)配制0.1 mol/L NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有_______(填写字母)。
A.称量氢氧化钠固体时砝码放反了 B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液 E.定容时俯视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。
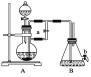
填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的离子方程式是___________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述生成Fe(OH)2的操作过程:________________________。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为__________________。
(5)下图中________能较长时间看到Fe(OH)2白色沉淀。
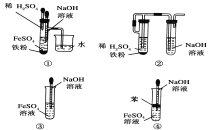
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,pH=2的两种一元酸HX、HY各取5 mL,分别加水稀释,溶液pH变化与所加水的体积关系如图所示(忽略混合溶液体积的变化),下列说法错误的是
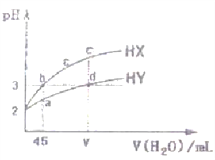
A. 分别取等体积a、b两点溶液,完全中和需同浓度NaOH溶液的体积V(HX)=V(HY)
B. b、d两点溶液中由水电离产生的H+浓度![]()
C. 相同条件下,a、b、c、d、e五点溶液的导电性大小顺序为:a>b=d>c>e
D. 加入NaOH溶液,可以使d点c(Y-)增大、c(H+)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com