
(1)下列实验操作可以达到实验目的的是 (填序号,多填扣分)(2分)
A.用铝片与四氧化三铁粉末混合加热进行铝热反应。
B.向蔗糖溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2检验水解产物。
C.用酸性高锰酸钾溶液能鉴别乙烷与乙烯。
D.用饱和Na2CO3溶液除去乙酸乙酯中的少量乙酸。
E.利用燃烧的方法可以鉴别出羊毛和棉花织品。
(2)请将下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法)。(6分)
a、蒸馏 b、裂解 c、过滤 d、裂化 e、干馏 f、分馏 g、电解 h、皂化
①把煤转化为焦炉气、煤焦油和焦炭等 ;
②从原油中分离出汽油、煤油、柴油等 ;
③将重油转化为汽油 ;
④将海水淡化 ;
⑤从海水得到的无水MgCl2中制取金属镁 ;
⑥用油脂制取肥皂_________________。
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子充数之和是Z的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
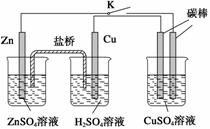
A.铜棒为正极,其电极反应式为2H++2e-===H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列MN,P物质,其中可以成立的是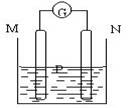
| M | N | P | |
| A | Zn | Cu | 稀硫酸 |
| B | Cu | Fe | 稀盐酸 |
| C | Ag | Zn | AgNO3溶液 |
| D | C | Fe | CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨。现取不同质量的该铝热剂分别和100mL同浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如下表(气体体积均在标准状况下测定)。
| ① | ② | ③ | |
| 铝热剂质量/g | 7.5 | 18.0 | 20.0 |
| 气体体积/L | 3.36 | 6.72 | 6.72 |
(1)该铝热反应的化学方程式为___________________________ (1分)
(2)该铝热剂中加入NaOH溶液时发生反应的化学方程式为_____________ (1分)
(3)求NaOH溶液的物质的量浓度:(3分)
(4)求该铝热剂中铝的质量分数。(3分)
查看答案和解析>>
科目:高中化学 来源: 题型:
电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1个,Y的最外层电子数比K层多1个,Z的单质常用于制造太阳能电池,W的原子半径 是同周期主族元素中最小的。下列推断中正确的是( )
是同周期主族元素中最小的。下列推断中正确的是( )
A.Z的简单氢化物的热稳定性强于W的简单氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的简单离子半径依次增大
D.X、Y、W的最高价氧化物对应的水化物之间互相都能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项表述,正确的是( )
A. 互为同系物
B.2,2,4,4四甲基己烷若由炔烃加氢而来,则该炔烃为2,2,4,4四甲基1己炔
C.当降冰片烷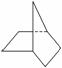 发生一氯取代时,能生成3种沸点不同的产物
发生一氯取代时,能生成3种沸点不同的产物
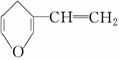 |
D.与 互为同分异构体的芳香族化合物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
“烂版液”是制印刷锌版时,用稀硝酸腐蚀锌版后得到的“废液”(含有少量的Cl-、Fe3+)。某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:

已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是______(填化学式,下同)。
(2)在操作①中保持pH=8的目的是__________________________________________。
(3)沉淀Ⅰ的主要成分是____________。
(4)操作③中加热煮沸的目的是________________;此步操作的理论依据是
________________________________________________________________________。
(5)操作④保持pH=2的目的是____________;此步操作中所用的主要仪器是
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com