
 硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义.利用硫铁矿烧渣制备铁红等产品的实验流程如下:
硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义.利用硫铁矿烧渣制备铁红等产品的实验流程如下:
 2Fe2O3+4CO2;因实验室进行煅烧操作所需仪器有酒精灯、泥三角、三脚架、玻璃棒、坩埚、坩埚钳,
2Fe2O3+4CO2;因实验室进行煅烧操作所需仪器有酒精灯、泥三角、三脚架、玻璃棒、坩埚、坩埚钳, 2Fe2O3+4CO2; 坩埚、坩埚钳;
2Fe2O3+4CO2; 坩埚、坩埚钳;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:安徽省模拟题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:山东省模拟题 题型:实验题
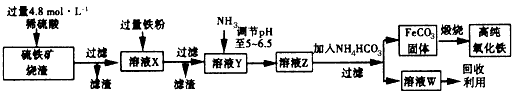
请回答下列问题:
(1)实验室用18.4 mol/L的浓硫酸配制250 mL 4.8 mol/L的硫酸溶液,所用的玻璃仪器除胶头滴管、量筒、烧杯、玻璃棒和酸式滴定管外,还需____ (填写仪器名称)。
(2)溶液X中加入铁粉后可能发生反应的离子方程式为____________________。
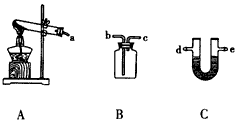
(3)某同学选用下列装置来制备纯净干燥的氨气,请完成下列有关问题
查看答案和解析>>
科目:高中化学 来源: 题型:
[s1] 用硫铁矿烧渣(主要成分为铁的氧化物和少量SiO2)为原料制取无机高分子絮凝剂聚合硫酸铁(PFS)的实验流程如下:
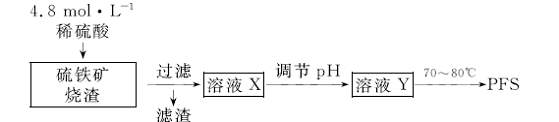
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需 。
(2)滤渣的主要化学成分是
(3)向溶液X中加入过量的铁粉后过滤,滤液经浓缩、结晶可制得绿矾,加入铁粉后发生的主要反应的离子方程式为 。
(4)溶液Y的pH影响产品中铁的质量分数,用pH试纸测定溶液pH的操作方法是 。若溶液Y的pH偏小,所得PF、S中铁的质量分数将偏 (填“高”或“低”)。
[s1]16.
查看答案和解析>>
科目:高中化学 来源:???????????2011?????????ε??п??? 题型:填空题
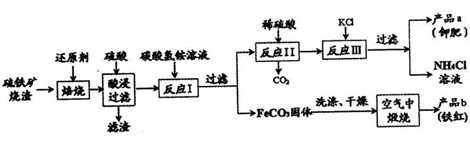
硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红等产品的流程如下图所示:

(1)硫铁矿烧渣焙烧时所添加的还原剂最有可能的是 。(填字母)
A.铝 B.锌 C.碳
(2)酸浸、过滤后滤液中的主要成分是 。
(3)反应Ⅰ的反应温度一般需控制在35℃以下,其目的是 。
(4)空气中煅烧FeCO3生成产品b的化学反应方程式为 。
(5)检验产品a中是否含有氯化物杂质的实验操作是:取少量产品a于试管中配成溶液, 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com