
·ÖĪö £Ø1£©øł¾Żn=cVŗĶm=nMĄ“¼ĘĖć£»
£Ø2£©ŅņĪŖ×īŗóŠčµßµ¹Ņ”ŌČ£¬ĖłŅŌČŻĮæĘæŌŚŹ¹ÓĆĒ°±ŲŠė¼ģ²éŹĒ·ńĀ©Ė®£»
£Ø3£©·ÖĪö²Ł×÷¶ŌČÜÖŹµÄĪļÖŹµÄĮænŗĶČÜŅŗµÄĢå»żV£¬ŅĄ¾Żc=$\frac{n}{V}$½ųŠŠĪó²ī·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©ÅäÖĘ250mL 1.25mol/LµÄNaOHČÜŅŗ£¬ŠčŅŖµÄNaOHµÄĪļÖŹµÄĮæn=cV=1.25mol/L”Į0.25L=0.3125mol£¬ŠčŅŖµÄÖŹĮæm=nM=0.3125mol”Į40g/mol=12.5g£¬
¹Ź“š°øĪŖ£ŗ12.5g£»
£Ø2£©ŅņĪŖ×īŗóŠčµßµ¹Ņ”ŌČ£¬ĖłŅŌČŻĮæĘæŌŚŹ¹ÓĆĒ°±ŲŠė¼ģ²éŹĒ·ńĀ©Ė®£»
¹Ź“š°øĪŖ£ŗ²éĀ©£»
£Ø3£©A£®³ĘĮæNaOHŹ±£¬ķĄĀė“ķ·ÅŌŚ×óÅĢ£ØŅŃŅʶÆÓĪĀė£©£¬µ¼ÖĀ³ĘĮæµÄĒāŃõ»ÆÄĘÖŹĮæĘ«Š”£¬ÅäÖʵÄČÜŅŗµÄÅضČĘ«Š”£¬¹ŹAÕżČ·£»
B£®ĻņČŻĮæĘæÖŠ×ŖŅĘČÜŅŗŹ±²»É÷ÓŠŅŗµĪČ÷ŌŚČŻĮæĘæĶāĆę£¬µ¼ÖĀĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĘ«Š”£¬ÅäÖʵÄČÜŅŗÅضČĘ«Š”£¬¹ŹBÕżČ·£»
C£®¶ØČŻŹ±ø©ŹÓæĢ¶ČĻߣ¬µ¼ÖĀ¼ÓČėµÄÕōĮóĖ®Ģå»żĘ«Š”£¬ÅäÖʵÄČÜŅŗÅضČĘ«øߣ¬¹ŹC“ķĪó£»
D£®ÅäÖĘĒ°£¬ČŻĮæĘæÖŠÓŠÉŁĮæÕōĮóĖ®£¬¶ŌČÜÖŹµÄĪļÖŹµÄĮæ¼°×īÖÕČÜŅŗĢå»żĆ»ÓŠÓ°Ļģ£¬²»Ó°ĻģÅäÖĘ½į¹ū£¬¹ŹD“ķĪó£»
E£®¶ØČŻŗó¾Õńµ“”¢Ņ”ŌČ£¬·¢ĻÖŅŗĆęĻĀ½µ£¬ŌŁ¼ÓŹŹĮæµÄÕōĮóĖ®ÖĮæĢ¶ČĻߣ¬µ¼ÖĀ¼ÓČėµÄÕōĮóĖ®Ģå»żĘ«“ó£¬ÅäÖʵÄČÜŅŗÅضČĘ«µĶ£¬¹ŹEÕżČ·£»
¹Ź“š°øĪŖ£ŗABE£®
µćĘĄ ±¾Ģāæ¼²éĮĖŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗÅäÖĘĪó²īµÄ·ÖĪö£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·ÅäÖĘŌĄķ½įŗĻc=$\frac{n}{V}$½ųŠŠ·ÖĪö²śÉśµÄĪó²ī£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£® +2NaOH$”ś_{”÷}^{“¼}$
+2NaOH$”ś_{”÷}^{“¼}$ +2NaBr+2H2O£®
+2NaBr+2H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ½«Ņ»¶ØÖŹĮæµÄMgŗĶAlµÄ»ģŗĻĪļĶ¶Čė2.0mol•L-1£¬250mLĻ”ĮņĖįÖŠ£¬¹ĢĢåČ«²æČܽā²¢²śÉśĘųĢ壮“ż·“Ó¦ĶźČ«ŗó£¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėNaOHČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼Ź¾£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
½«Ņ»¶ØÖŹĮæµÄMgŗĶAlµÄ»ģŗĻĪļĶ¶Čė2.0mol•L-1£¬250mLĻ”ĮņĖįÖŠ£¬¹ĢĢåČ«²æČܽā²¢²śÉśĘųĢ壮“ż·“Ó¦ĶźČ«ŗó£¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėNaOHČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼Ź¾£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | µ±¼ÓĒāŃõ»ÆÄĘČÜŅŗĢå»żĪŖ20mLŹ±£¬ČÜŅŗµÄpHÖµµČÓŚ7 | |
| B£® | µ±¼ÓĒāŃõ»ÆÄĘČÜŅŗĢå»żĪŖ20mLŹ±£¬ČÜŅŗÖŠµÄČÜÖŹÖ»ÓŠĮņĖįĆ¾ŗĶĮņĖįĀĮ | |
| C£® | NaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ5 mol•L-1 | |
| D£® | Éś³ÉµÄH2ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ11.2L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
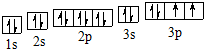 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| ·“Ó¦ĪļĶ¶ČėĮæ | 2molSO2”¢1molO2 | 1molSO2”¢0.5molO2 | 2molSO3 |
| k1 | k2 | k3 | |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | ·Å³öakJ | ·Å³öbkJ | ĪüŹÕckJ |
| ĘųĢåĆÜ¶Č | ¦Ń1 | ¦Ń2 | ¦Ń3 |
| ·“Ó¦Īļ×Ŗ»ÆĀŹ | ¦Į1 | ¦Į2 | ¦Į3 |
| A£® | k1=k3£¼k2 | B£® | ¦Ń1=¦Ń3£¾¦Ń2 | C£® | ¦Į2+¦Į3£¾1 | D£® | 2b+c£¾197 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
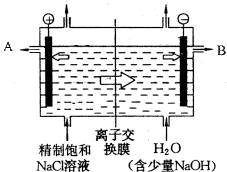 ¹¤ŅµÉĻµē½āÖĘÉÕ¼īµÄ¼¼ŹõŹĒÓĆĄė×Ó½»»»Ä¤·Ø£¬Ö÷ŅŖŌĮĻŹĒ±„ŗĶŹ³ŃĪĖ®£®Ķ¼ĪŖĄė×Ó½»»»Ä¤·Øµē½āŌĄķŹ¾ŅāĶ¼£ŗ
¹¤ŅµÉĻµē½āÖĘÉÕ¼īµÄ¼¼ŹõŹĒÓĆĄė×Ó½»»»Ä¤·Ø£¬Ö÷ŅŖŌĮĻŹĒ±„ŗĶŹ³ŃĪĖ®£®Ķ¼ĪŖĄė×Ó½»»»Ä¤·Øµē½āŌĄķŹ¾ŅāĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µĆ³öĶźÕūµÄŌŖĖŲÖÜĘŚ±ķ | B£® | ·¢ĻÖĮĖŌŖĖŲÖÜĘŚĀÉ | ||
| C£® | ·¢ĻÖæÕĘųµÄ×é³É | D£® | Ģį³öŌ×Ó”¢·Ö×ÓѧĖµ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2+O2$\frac{\underline{\;µćČ¼\;}}{\;}$2H2O | B£® | CO2+H2OØTH2CO3 | ||
| C£® | Fe+H2SO4ØTFeSO4+H2”ü | D£® | MgCO3+2HClØT2MgCl2+CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com