
【题目】下列中学常见实验的现象或表述正确的是![]()
A.饱和碳酸钠溶液和饱和碳酸氢钠溶液中滴入酚酞溶液,溶液均显红色
B.含4molHCl的浓盐酸与足量的![]() 共热,得到
共热,得到![]()
C.铝箔在空气中用酒精灯加热可以熔化滴落,且发生剧烈燃烧
D.![]() 和
和![]() 的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是
的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是![]() 和
和![]()
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)乙烯的电子式_________________。
(2)![]() 的分子式_________________。
的分子式_________________。
(3)![]() 的键线式___________________。
的键线式___________________。
(4)![]() 的系统命名为__________________。
的系统命名为__________________。
(5)分子式为C8H8O,遇FeCl3溶液显紫色且苯环上还有1个烃基的同分异构体有___种。
(6)C4H10O的同分异构体中,属于醇类且含有“手性碳原子”的结构简式为_________。
(7)CH2=CH-CH3加聚产物是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入 1 mol X 与 2 mol Y 发生反应:X(g)+2Y(g) ![]() aZ(g) H<0,达到平衡后,改变某一条件(温度或容器体积),X 的平衡转化率的变化如图所示。下列说法中正确的是( )
aZ(g) H<0,达到平衡后,改变某一条件(温度或容器体积),X 的平衡转化率的变化如图所示。下列说法中正确的是( )
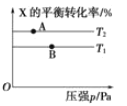
A.a=2
B.T2>T1
C.A 点的反应速率:3v 正(X)=v 逆(Z)
D.用 Y 表示 A、B 两点的反应速率:v(A)>v(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,下图是利用手持技术得到的微粒物质的量变化图,常温下向![]() 溶液中滴加
溶液中滴加![]() 溶液.下列说法正确的是
溶液.下列说法正确的是![]()

A.![]() A在水中的电离方程式是:
A在水中的电离方程式是:![]()
![]()
![]() ;HA
;HA![]()
B.当![]() 时,则有:
时,则有:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
C.当![]() 时,则有:
时,则有:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
D.当![]() 时,其溶液中水的电离受到抑制
时,其溶液中水的电离受到抑制
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下pH均为2的两种酸溶液X和Y各10 mL分别加水稀释到10000 mL,其pH与所加水的体积变化如图所示,下列结论中正确的是

A.加水后,Y酸的电离度增大
B.X酸在水溶液中存在电离平衡
C.加水后,X酸的电离平衡常数减小
D.X酸的物质的量浓度与Y酸的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取20 mL某浓度的盐酸作为待测液,用-定物质的量浓度的NaOH溶液进行滴定(溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示。下列叙述不正确的是( )
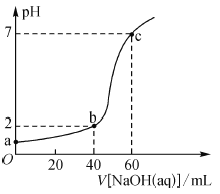
A.盐酸与NaOH溶液初始浓度关系为c(HCl)-2c(NaOH)=0.03mol·L-1
B.b点溶液中:c(Cl-)>c(Na+)>c(H+)>c(OH-)
C.a、b、c点溶液中水的电离程度大小依次为:a>b>c
D.滴定前,锥形瓶用待测液润洗,会导致所测HCl浓度偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A和B反应的化学方程式为A(g)+2B(g)![]() C(g)。回答下列问题:
C(g)。回答下列问题:
(1)图1是反应A(g)+2B(g)![]() C(g)在不同温度下A的转化率随时间变化的曲线。
C(g)在不同温度下A的转化率随时间变化的曲线。
①该反应的△H___(填“>”“<”或“=”)0。
②T1和T2温度下的平衡常数大小关系是K1___(填“>”“<”或“=”)K2。在T1温度下,向体积为1L的密闭容器中,充入1molA(g)和2molB(g),测得A(g)和C(g)的浓度随时间变化如图2所示。则该反应的平衡常数为___。

③若容器容积不变,下列措施可增加A转化率的是___(填字母)。
a.升高温度 b.将C(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)在容积为1L的恒容密闭容器中,分别研究在230°C、250℃和270℃条件下的上述反应。三种温度下B与A的物质的量之比与A平衡转化率的关系如图3所示。曲线z对应的温度是___℃;该温度下,若反应物A的物质的量为1 mol,则该反应的化学平衡常数为___(用分数表示)。曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电导率传感器可绘制电导率曲线图,下图为用0.1mol/LNaOH溶液滴定10mL0.lmol/L盐酸过程中的电导率曲线。下列说法错误的是

A. 电导率传感器能用于判断酸碱中和滴定的终点
B. a、b、c 点的溶液中,离子浓度由大到小顺序为a>b>c
C. d点所示溶液中存在:c(Cl-) +c(OH-) =c(H+) +c(Na+)
D. C点电导率最小是因为此时溶液中导电微粒数目最少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
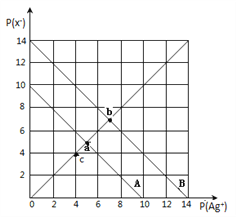
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com