


科目:高中化学 来源: 题型:
| A、1:1 | B、1:2 |
| C、2:3 | D、3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
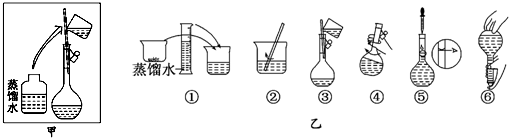
| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
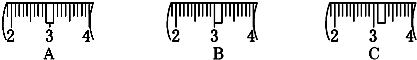
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、以铝为阳极、铜为阴极电解硫酸铜溶液时,阳极铝溶解 |
| B、与氯气反应时,铝失去3个电子,而铜失去2个电子 |
| C、常温下,铝在浓硝酸中钝化而铜不发生钝化 |
| D、常温下将铝和铜用导线连接放入到稀盐酸中,铝为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2molKClO3 |
| B、1mol KCl |
| C、2molMgCl2 |
| D、2molNaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法不正确的是( )| A、电流从右侧电极经过负载后流向左侧电极 |
| B、为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| C、电极A极反应式为:2NH3-6e-=N2+6H+ |
| D、当有4.48L NO2(标准状况) 被处理时,转移电子为0.8mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com