
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他材料电池,电池总反应为V2O5+xLi LixV2O5。下列说法中正确的是
LixV2O5。下列说法中正确的是
A.电池在放电时,Li+向负极移动
B.锂在放电时做正极,充电时为阳极
C.该电池充电时阳极的反应为LixV2O5﹣xe-═V2O5+xLi+
D.V2O5只是锂发生反应的载体,不参与电池反应
科目:高中化学 来源:2015届湖南省高三第二次月考化学试卷(解析版) 题型:填空题
(16分)2014年3月22日是第二十二届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的_______倍。
(2)炼金废水中含有络离子[Au(CN)2]+,与弱电解质碳酸的电离方式相似,[Au(CN)2]+也存在着两步电离,其电离出CN-有毒,CN-与H+结合生成毒性更强的HCN。 [Au(CN)2]+的一级电离方程式: ;在碱性条件下NaClO将废水中的CN-氧化成CO和N2,其反应的离子方程式为: 。
(3)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如下图所示:

请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为________________。
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为_________________ ___。
③试确定NO3-是否存在?_________________(填“存在”、“不存在”或“不确定”),若存在,试计算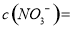 _________________(若不存在,此问不必作答)。
_________________(若不存在,此问不必作答)。
(4)聚合硫酸铁又称聚铁,其化学式为[Fe2(OH)n(SO4)(3―0.5n)]m(n>2,m≤10),它是一种高效的无机高分子混凝剂、净水剂。 某中学化学兴趣小组查资料获取测定聚铁中含铁量的方法:把聚铁溶于过量酸中,先用过量SnCl2将Fe3+还原成 Fe2+:Sn2+ + 2Fe3+ + 6Cl-= 2Fe2+ + SnCl62-,再加入HgCl2溶液除去过量的SnCl2:Sn2+ + 2Hg2+ + 8Cl- = Hg2Cl2↓+ SnCl62-,然后用标准的K2Cr2O7溶液(先加入几滴试亚铁灵指示剂)滴定溶液中的Fe2+。若称取聚铁质量为10.00g配成100.0 mL溶液,取出20.00 mL,经上述方法处理后,再用0.1000 mol·L—1K2Cr2O7标准溶液滴定,达到终点时,消耗标准溶液12.80 mL,则聚铁中铁元素的质量分数为 %。(保留小数点后一位)
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高一上学期期中考试化学试卷(解析版) 题型:填空题
硫酸试剂瓶标签上的部分内容如图。
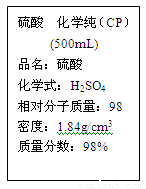
据此回答下列问题:
(1)该硫酸的物质的量浓度为 mol/L。
(2)配制250mL 0.50mol·L-1的稀硫酸需取该硫酸 mL。
(3)配制时必需的玻璃仪器有: 。
(4)定容时,若加入的水超过刻度线,必须采取的措施是 。
(5)下列操作会使所配溶液浓度偏低的是 。
A.转移溶液时,未洗涤烧杯
B.容量瓶用蒸馏水洗净后仍残留蒸馏水
C.定容时,俯视容量瓶的的刻度线
D.定容摇匀后,发现液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高一上学期期中考试化学试卷(解析版) 题型:选择题
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是

A.Cl2+2KBr = Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4NO2+O2+2H2O = 4HNO3
D.2Na2O2+2CO2 = 2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三十月阶段性考试化学试卷(解析版) 题型:填空题
(10分)A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
阳离子 | Na+、Al3+、Ba2+、NH4+ |
阴离子 | Cl-、OH-、CO32-、SO42- |
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试纸变蓝
回答下列问题:
(1)A的化学式是_________,用电子式表示C的形成过程:________________ 。
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,所得溶液中各离子物质的量浓度由大到小的顺序是:________________________ 。
(3)写出③的离子方程式_______________________________________________ 。
(4)简述D溶液呈碱性的理由___________________________________________ 。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三十月阶段性考试化学试卷(解析版) 题型:选择题
在一定温度下向饱和Na2SO4溶液中加入ag无水硫酸钠粉末,搅拌,静置后析出bg Na2SO4·10H2O晶体,(b-a)g是
A.原饱和溶液失去的水的质量 B.原饱和溶液中减少的硫酸钠的质量
C.原饱和溶液中失去的水和硫酸钠的总质量 D.析出的晶体含有的硫酸钠的质量
查看答案和解析>>
科目:高中化学 来源:2015届湖北省四校高三上学期期中联考化学试卷(解析版) 题型:填空题
(8分)钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为 ;步骤③中反应的离子方程式为: 。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将 (填“偏高”、或“偏低”或“不变”)。
(3)在步骤③中,需要 1.00 mol·L-1氢氧化钠标准溶液450mL,配制该溶液需用托盘天平称取___gNaOH固体。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省四校高三上学期期中联考化学试卷(解析版) 题型:选择题
下列有关物质的性质、制取或应用等的说法中正确的是( )
A.用8%的盐酸蒸发浓缩获得30%的盐酸
B.光纤和餐桌上的瓷盘都是硅酸盐制品
C.可利用丁达尔效应来区别淀粉溶液和氯化钠溶液
D.二氧化硫具有漂白性,与氯水混合使用漂白效果更好
查看答案和解析>>
科目:高中化学 来源:2015届海南省高三第四次月考化学试卷(解析版) 题型:选择题
常温下a mol/L CH3COOH稀溶液和b mol/L KOH 稀溶液等体积混合,下列判断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CH3COO-),a<b
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CH3COO-),a<b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com