
| A. | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | |
| B. | 用煤气灶燃烧天然气为炒菜提供热量 | |
| C. | 牛奶久置空气中变质腐败 | |
| D. | 向沸水中滴入FeCl3饱和溶液,适当加热,制备胶体 |
分析 有元素化合价变化的反应属于氧化还原反应,没有元素化合价变化的反应则不属于氧化还原反应.
解答 解:A、铁锅,经放置常出现红棕色斑迹,则铁元素的化合价升高被氧化,发生氧化还原反应,故A不选;
B、用煤气灶燃烧沼气,碳元素的化合价升高,氧元素的化合价降低,发生氧化还原反应,故B不选;
C、牛奶久置变质腐败,氧元素的化合价降低,则发生氧化还原反应,故C不选;
D.向沸水中滴入FeCl3饱和溶液,是铁离子的水解,没有元素的化合价变化,则不属于氧化还原反应,故D选;
故选D.
点评 本题考查氧化还原反应与厨房中的化学知识,明确生活中的现象及发生的对应的化学变化是解答本题的关键,并利用化合价来分析是否为氧化还原反应.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
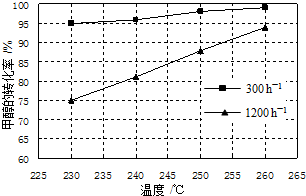 以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向.
以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
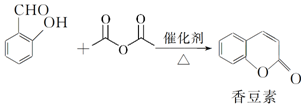

 ;
; 和
和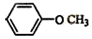 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

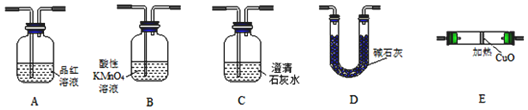
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的平衡常数K1=4.2×10-7 | |
| B. | 少量Cl2通入到过量的Na2CO3溶液的离子方程式为Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO- | |
| C. | Cl2与Na2CO3按物质的量之比1:1恰好反应的离子方程式为Cl2+CO32-+H2O═HCO3-+Cl-+HClO | |
| D. | 少量CO2通入到过量的NaClO溶液的离子方程式为2ClO-+CO2+H2O═CO32-+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com