
| A�� | ԭ�Ӱ뾶��C��D��B��A | |
| B�� | C��B�γɵ����ֻ�������������ӻ�����һ�ѧ��������ȫ��ͬ | |
| C�� | �����̬�⻯����ȶ��ԣ�B��A | |
| D�� | A��D��E������������Ӧˮ�������������ǿ |
���� A��B��C��D��E�Ƕ�������ԭ���������������5������Ԫ�أ�����A������л���ı�ҪԪ�أ���AΪC��Ԫ��D��AΪͬ��Ԫ�أ���DΪSi��Ԫ��B��ԭ������������������Ӳ�����3��������Ӳ���Ϊ2������������Ϊ6������BΪO��Ԫ��C��E�γɵĻ�����CE�dz������õ�ζƷ��CEΪNaCl�����ԭ��������֪CΪNa��EΪCl��Ȼ����Ԫ�ؼ��仯��������������
��� �⣺�����Ϸ�����֪ΪAΪC��BΪO��CΪNa��DΪSi��EΪClԪ�أ�
A��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С�����Ӳ�Խ��뾶Խ������ԭ�Ӱ뾶ΪNa��Si��Cl��C��O����C��D��E��A��B����A����
B��C��B�γɵ����ֻ�����ΪNa2O��Na2O2��Na2O��ֻ�����Ӽ�����Na2O2�������Ӽ��ͷǼ��Թ��ۼ�����B����
C���ǽ�����O��C��Ԫ�صķǽ�����Խǿ����Ӧ���⻯��Խ�ȶ�����C��ȷ��
D��A��D��E������������Ӧˮ����ֱ�ΪH2CO3��H2SiO3��HClO4���ǽ�����Cl��C��Si��������H2SiO3��H2CO3��HClO4����D����
��ѡC��
���� ���⿼��λ�á��ṹ�����ʵ�Ӧ�ã�Ϊ��Ƶ���㣬����Ԫ�ص�λ�á�Ԫ�ػ�����֪ʶ�ƶ�Ԫ��Ϊ���Ĺؼ������ط������ƶ������Ŀ��飬ע��Ԫ�������ɼ�Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͭ��Ӧ�õ�NO2��N2O4��23g����ͭʧȥ�ĵ�����Ϊ0.5NA | |
| B�� | 10g 46%���Ҵ�ˮ��Һ��������ԭ����ĿΪ0.6NA | |
| C�� | ��״����8.96L��ƽ����Է�������Ϊ3.5��H2��D2����������0.3NA | |
| D�� | 1molCu��������S��ȫ��Ӧ��ת�Ƶ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
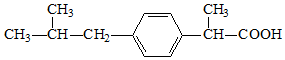
| A�� | ����ҵķ���ʽΪC13H18O2 | |
| B�� | ������뱽������ͬϵ�� | |
| C�� | 1mol ������������3mol ���������ӳɷ�Ӧ | |
| D�� | ������ڱ����Ϸ���ȡ����Ӧ����һ�ȴ�����4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
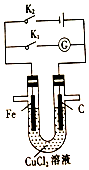
| A�� | ͬʱ��K1��K2�����������Ϻ�ɫ�������� | |
| B�� | ֻ�պ�K1��ʯī�������Ϻ�ɫ�������� | |
| C�� | ֻ�պ�K2������·��ͨ��0.3mol����ʱ������������4.48L����״�������� | |
| D�� | ֻ�պ�K2��һ��ʱ����������Һ������ȣ���Һ��pH�������Cl2���ܽ⣩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16 g O2��O3 �Ļ�������к��еķ�����Ϊ0.5 NA | |
| B�� | 25��ʱ��Ksp��BaSO4��=1��10-10����BaSO4������Һ��Ba2+����Ϊ1��10-5 NA | |
| C�� | ��״���£�2.24 L Cl2 ͨ������H2O��NaOH��Һ��ת�Ƶĵ�������Ϊ0.1 NA | |
| D�� | �����£�1 mol��NaHCO3�����к�HCO3-����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
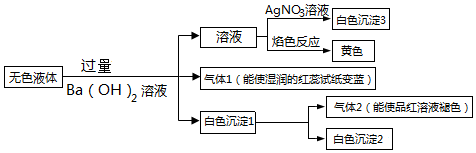
| A�� | ����2һ����SO2 | B�� | ��ɫ����2һ����BaSO4 | ||
| C�� | ��ɫ����1�ijɷ�ֻ��2�ֿ��� | D�� | ��Һ��ֻ��HCO3-��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
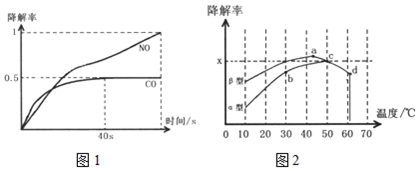
 ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɱ����ڿ��������� | B�� | ����ʹʯӢ�ۻ� | ||
| C�� | ��ʳ���ܽ���ˮ | D�� | ����ʹ����ֽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com