
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.03mol/L |
| D、0.04mol/L |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
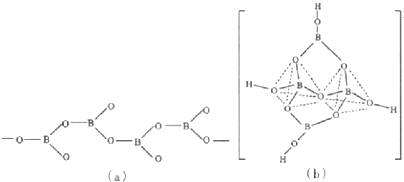
| 化学键 | B-H | B-0 | B-B |
| 键能(kj?mol-1) | 389 | 561 | 293 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此时反应物B全部转化成了生成物 |
| B、单位时间内生成n mol A,同时生成4n mol C |
| C、若改变条件,A、B、C的浓度不可能再变化 |
| D、A、B、C的分子数比为1:3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④②③①⑤ |
| B、②④①⑤③ |
| C、①③⑤②④ |
| D、④②①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
| C、c(H+) | ||
| D、n(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时,单位时间内n(B)消耗﹕n(C)消耗=1﹕1 |
| B、若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体 |
| C、升高温度,C百分含量减少,说明正反应是放热反应 |
| D、增大压强,平衡不移动,说明B是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、被氧化的物质是氧化剂 |
| B、可以利用酒精将碘水中的碘提取出来 |
| C、化合反应一定不是氧化还原反应 |
| D、铝抗腐蚀是外层氧化膜致密的缘故 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1 |
| B、0.01mol?L-1 |
| C、0.2mol?L-1 |
| D、0.02mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu能导电,所以Cu是电解质 |
| B、NaCl溶液导电,所以NaCl溶液是电解质 |
| C、SO2溶于水能导电,所以SO2是电解质 |
| D、熔融状态的Na2O导电,所以Na2O是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com