
科目:高中化学 来源: 题型:

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| a |
| 10 |
| 1.45 |
| a |
| 1.45 |
| a |
| 1.40 |
| a |
| 1.40 |
| a |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、碱
性、澄清溶液的是 ( )
A.Na+、Al3+、Cl-、OH-(5∶2∶7∶4)
B.NH![]() 、Ba2+、OH-、Cl-(1∶1∶1∶2)
、Ba2+、OH-、Cl-(1∶1∶1∶2)
C.Fe3+、Na+、Cl-、S2-(1∶2∶3∶1)
D.K+、H+、I-、HCO![]() (1∶1∶1∶1)
(1∶1∶1∶1)
查看答案和解析>>
科目:高中化学 来源:宜宾模拟 题型:问答题
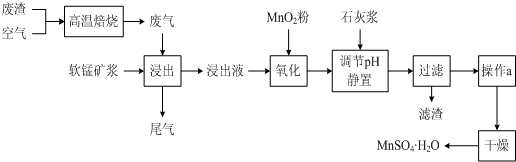
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:2010年四川省宜宾市高考调研化学试卷(解析版) 题型:解答题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com