
| A、新制氯水中加入固体氢氧化钠后,溶液中有c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | ||
B、加水稀释0.2 mol?L-1的醋酸溶液后,溶液中
| ||
| C、pH=3的弱酸HR溶液与pH=13的NaOH溶液等体积混合后,恰好完全反应,反应后的溶液中一定有:c(R-)+c(HR)=0.05mol?L-1 | ||
| D、0.2 mol?L-1的CH3COOH溶液与0.1 mol?L-1NaOH溶液等体积混合后溶液呈酸性,则c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
| c(CH3COO-) |
| c(CH3COOH).c(OH-) |
| c(CH3COO-).c(H+) |
| c(CH3COOH).c(OH-).c(H+) |
| Ka |
| Kw |
| c(CH3COO-) |
| c(CH3COOH).c(OH-) |


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:

| A、电子通过外电路从b极流向a极 |
| B、H+由a极通过固体酸电解质传递到b极 |
| C、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| D、每转移0.1mol电子,消耗1.12L的H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH值变大 |
| B、n (OH-)减少 |
| C、C (Ca2+)增大 |
| D、pH值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol/L |
| B、1.5mol/L |
| C、3mol/L |
| D、7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na与水反应比与C2H5OH反应强烈 |
| B、丙酮(CH3COCH3)分子中的氢原子比乙烷分子中的氢原子更易被卤素原子取代 |
| C、甲酸的酸性比乙酸强 |
| D、相等质量的甲醇和乙醇分别与足量金属钠反应,甲醇产生的H2更多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝加到热水中 |
| B、NaAlO2溶液中加入足量CO2 |
| C、铝投入氨水中 |
| D、NaOH溶液中滴入少量AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示的物质或概念间的从属关系中不正确的是( )
如图表示的物质或概念间的从属关系中不正确的是( )| X | Y | Z | |
| A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 置换反应 | 氧化还原反应 | 离子反应 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
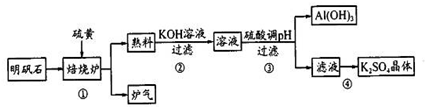
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com