
钛的化合物如TiO2、Ti(NO3)4、TiCl4、 Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式____________。
(2)TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4-中B原子的杂化类型为____________;
(3)在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子化学式为_________________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2•H2O(绿色),两者配位数_____(填“相同”或“不同”),绿色晶体中配体是______。
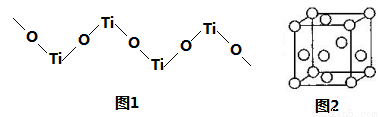
(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为____________。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为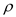 g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
科目:高中化学 来源:江西省新余市、宜春中学2017届高三下学期开学联考理科综合-化学试卷 题型:推断题
1,6-己二酸(G)是合成尼龙的重要原料之一,可用六个碳原子的化合物氧化制备.如图为A通过氧化反应制备G的反应过程(可能的反应中间物质为B、C、D、E和F).回答问题:
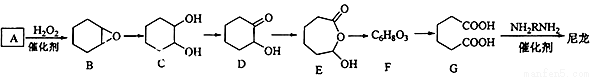
(1)化合物A中含碳87.8%,其余为氢,A的化学名称为__________________;
(2)B到C的反应类型为_______________;
(3)F的结构简式为___________________;
(4)在上述中间物质中,核磁共振氢谱中峰最多的是______,最少的是__________(填化合物代号,可能有多选)。
(5)由G合成尼龙的化学方程式为______________________;
(6)由A通过两步制备1,3﹣环己二烯的合成线路为______________(样式:A条件和试剂B一定条件 C)。
(7)有机物C的同分异构体属于酯类的有_________种.
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三第五次模拟化学卷(解析版) 题型:选择题
甲、乙、丙、丁、戊五种物质中,甲、乙、丙均含有相同的某种元素,丁是一种常见气体单质,它们之间具有如图所示转化关系。下列有关物质的推断不正确的是
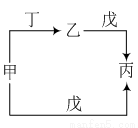
A.若甲为Na,则戊可能是H2O
B.若甲为C2H4,则戊可能是O2
C.若甲为NO,则戊可能是H2O
D.若甲为Cl2,则戊可能是NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试化学试卷(解析版) 题型:选择题
一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)  xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
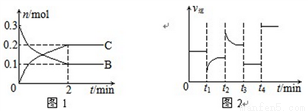
下列有关说法正确的是
A. x=2,反应开始2 min内,v(A)=0.05 mol/(L·min)
B. t1时改变的条件是降温,平衡逆向移动
C. t2时改变的条件可能是增大C的浓度,t2时正反应速率减小
D. t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试化学试卷(解析版) 题型:选择题
化学用语是学习化学的重要工具,下列化学用语中,正确的是
A. NH4+的水解反应离子方程式:NH4++H2O NH3•H2O+H+
NH3•H2O+H+
B. 在AgCl悬浊液中加入KI溶液充分振荡:Ag++I-=AgI↓
C. 镀铜时,阳极的电极反应式为:Cu2++2e-═Cu
D. 某反应△H<0,则该反应在任意条件下均可自发进行
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省牡丹江市高三2月开学检测理综化学试卷(解析版) 题型:选择题
下列实验“操作和现象”与“结论”及对应关系均正确的是
实验操作、现象 | 实验结论 | |
A | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置后CCl4层均有颜色 | 氧化性:Fe3+>Br2>I2 |
B | 向某溶液中加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量SO42- |
C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下 Ksp(BaCO3)>Ksp(BaSO4) |
D | 除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再放入CuSO4溶液中无现象 | 铁钉表面形成了一层致密稳定的氧化膜 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:简答题
钛白粉(金红石晶型 TiO2)被广泛用于制造高级白色油漆。工业上以钛铁矿(主要成分为 FeTiO3,含有 Fe2O3 和 SiO2 等杂质)为原料制钛白粉的主要工艺如下:
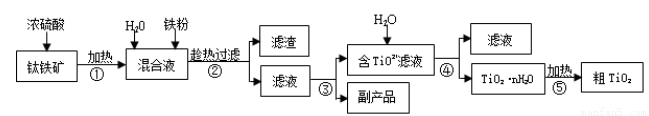
回答下列问题:
(1)第②步所得滤渣的成分是________。
(2)操作④中需要控制条件以形成 TiO2·nH2O 溶胶,该工艺过程若要在实验室里完成,其中的“过滤”操作,可选用下列装置________(填选项)。
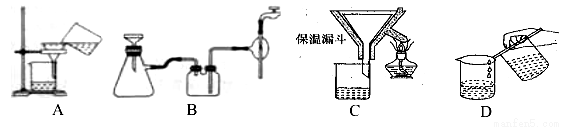
(3)第③步的实验操作是______、过滤,从而获得副产品 FeSO4·7H2O。
(4)为测定操作③所得滤液中TiO2+的浓度,取待测滤液10 mL 用蒸馏水稀释至100 mL,加入过量铝粉,充分振荡,使其完全反应:3TiO2+ + Al + 6H+ = 3Ti3+ + Al3+ + 3H2O。过滤后,取出滤液20.00 mL(加铝粉时引起溶液体积的变化忽略不计),向其中滴加2~3 滴KSCN溶液作指示剂,用 0.1000 mol·L-1NH4Fe(SO4)2 标准溶液滴定至溶液出现红色,此时溶液中 Ti3+全部被氧化为 Ti4+,消耗标准液30.00mL。回答下列问题:
①下列操作会使所测 TiO2+浓度偏高的是______。
A. 在配制标准液的过程中,未洗涤烧杯和玻璃棒
B. 在配制标准液定容是俯视刻度线
C.用蒸馏水洗涤后未经润洗的滴定管取待测液
D.在滴定终点读数时仰视滴定管刻度线
②求得待测滤液中 TiO2+的物质的量浓度是______。
(5)科学家从电解冶炼铝的工艺中得到启发,找出了冶炼钛的新工艺—TiO2 直接电解法生产钛,电解质为熔融的氯化钙,原理如图所示。

写出阴极电极反应式___________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A. 铁和盐酸溶液反应:2Fe + 6H+ === 2Fe3+ +3 H2↑
B. 氯气和水反应:Cl2 + H2O 2 H+ + Cl- + ClO
2 H+ + Cl- + ClO
C. 氢氧化钡溶液与硫酸铜溶液反应:Ba2+ + SO42- = BaSO4↓
D. 氯化铁溶液与氨水溶液反应: Fe3+ + 3 NH3·H2O === Fe (OH)3 ↓+ 3NH4+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二下学期开学考试化学试卷(解析版) 题型:选择题
下列有关四个常用电化学装置的叙述正确的是
|
|
|
|
图Ⅰ碱性锌锰电池 | 图Ⅱ铅-硫酸蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图II所示电池放电过程中,硫酸浓度不断增大
C. 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图IV所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com