
| A. | 氯气的水溶液能导电,所以氯气是电解质 | |
| B. | 干燥的氯气无漂白性,液氯具有极强的漂白性 | |
| C. | 氯气能使紫色石蕊溶液先变红后褪色 | |
| D. | 铜在氯气中燃烧生成红棕色烟 |
分析 A.电解质是在水溶液中或熔融状态下能导电的化合物,根据定义判断;
B、氯气的漂白是次氯酸的漂白,所以液氯也没有漂白性;
C、氯气与水反应生成HCl、HClO,溶液具有酸性和漂白性,以此来解答;
D、根据铜粉在氯气中燃烧的现象进行分析判断.
解答 解:A.氯气是非金属单质,不属于电解质,故A错误;
B、氯气的漂白是次氯酸的漂白,所以液氯也没有漂白性,故B错误;
C、氯气与水反应生成HCl、HClO,溶液具有酸性和漂白性,则紫色石蕊溶液先变红后褪色,故C正确;
D、铜粉在氯气中燃烧生成氯化铜,有大量棕黄色的烟产生,故D错误;
故选C.
点评 本题考查氯气的化学性质,为高频考点,把握氯气与水反应生成物的性质为解答的关键,侧重分析与应用能力的考查,注意HClO的漂白性,题目难度不大.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题
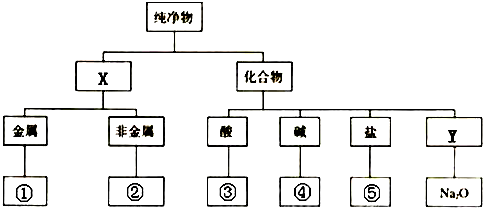
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
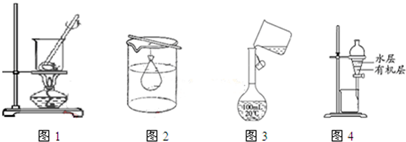
| A. | 图1:实验室灼烧胆矾测定胆矾中结晶水的含量 | |
| B. | 图2:除去Fe(OH)3胶体中的FeCl3 | |
| C. | 图3:向容量瓶中转移液体 | |
| D. | 图4:用苯萃取溴水中的Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入石灰石 | B. | 光照 | C. | 加入固体NaOH | D. | 加水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径由小到大的顺序是S2-、Na+、Mg2+ | |
| B. | 杂化轨道可用于形成σ键和π键 | |
| C. | Cu(NH3)4]2+中H提供接受孤对电子的空轨道 | |
| D. | 分子中心原子通过sp3杂化轨道成键时,该分子不一定为四面体构型 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
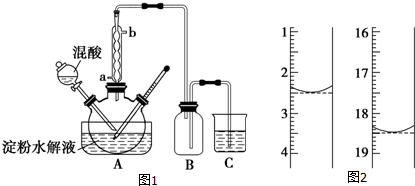
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com