
| A. | 将标准状况下1.12 L NH3溶于500 mL水中 | |
| B. | 将标准状况下1.12 L NH3溶于水配成500 mL溶液 | |
| C. | 取1 mol•L-1的氨水50 mL,加入500 mL水中 | |
| D. | 取1 mol•L-1的氨水100 mL,配成1 000 mL溶液 |
分析 A.溶液的体积不是500mL;
B.根据C=$\frac{n}{V}$解题;
C.根据不同液体混合时体积能否直接加和判断;
D.500mL容量瓶只能用来配制500ml溶液.
解答 解:A.体积指溶液体积不是溶剂体积,500mL水溶解氨气后体积增大,溶液的浓度小于0.1mol/L,故A错误;
B.将标准状况下1.12L的氨气的物质的量是0.05mol,根据C=$\frac{n}{V}$=$\frac{0.05mol}{0.5L}$=0.1mol/L,故B正确;
C.1mol/L的氨水50mL与500mL水混合配成溶液的体积不是500mL,所以混合后溶液的物质的量浓度不是0.1mol/L,故C错误;
D.500mL容量瓶只能用来配制500ml溶液,不能配成1000mL溶液,故D错误.
故选:B.
点评 本题考查了有关物质的量浓度的问题,难度不大,注意根据C=$\frac{n}{V}$解题.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 单位时间内消耗amolA,同时生成3amolC | |
| B. | 容器的压强不再变化 | |
| C. | 混合气体的物质的量不再变化 | |
| D. | C的生成速率与B的生成速率的比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
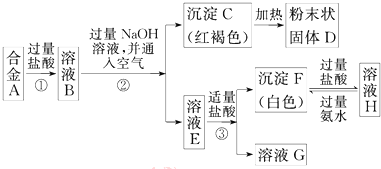
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某无色溶液中滴入石蕊试液后溶液呈蓝色,证明该溶液一定是碱的溶液 | |
| B. | 向某无色溶液中滴入硝酸银溶液产生白色沉淀,证明该溶液一定是盐酸 | |
| C. | 某白色固体与熟石灰混合研磨后产生有刺激性的氨味,证明该固体是铵盐 | |
| D. | 向某固体中加入稀盐酸产生气泡,证明该固体一定是碳酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,其中S原子轨道的杂化类型是sp3,它是极性(填“极性”或“非极性”)分子.
,其中S原子轨道的杂化类型是sp3,它是极性(填“极性”或“非极性”)分子.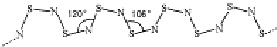
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质分子中均存在化学键 | |
| B. | 含有共价键的化合物不一定是共价化合物 | |
| C. | 阴阳离子间通过静电引力而形成的化学键叫做离子键 | |
| D. | 只有金属元素和非金属元素化合时才能形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
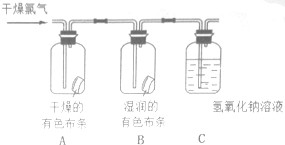 为了验证氯气的有关行政,某同学设计了如下的实验.
为了验证氯气的有关行政,某同学设计了如下的实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
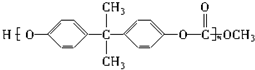 中含有
中含有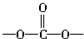 结构.
结构.| A. | ②⑤ | B. | ②④⑥ | C. | ①②③⑥ | D. | ②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com