
 .
.分析 短周期元素X、Y、Z、W、Q的原子序数依次增大.Y原子最外层电子数是次外层的2倍,Y有2个电子层,最外层电子数为4,则Y为碳元素;Q的单质是常见的半导体材料,则Q为Si元素;W是金属,X、W可分别与Z形成原子个数比1:1和2:1两种化合物,则X为氢元素、Z为氧元素、W为Na元素,据此解答.
解答 解:短周期元素X、Y、Z、W、Q的原子序数依次增大.Y原子最外层电子数是次外层的2倍,Y有2个电子层,最外层电子数为4,则Y为碳元素;Q的单质是常见的半导体材料,则Q为Si元素;W是金属,X、W可分别与Z形成原子个数比1:1和2:1两种化合物,则X为氢元素、Z为氧元素、W为Na元素,
(1)Q为Si元素,碳原子有3个电子层,最外层电子数为4,处于元素周期表中第三周期第ⅣA族,
故答案为:第三周期第ⅣA族;
(2)YZ2是CO2,属于共价化合物,它的电子式为 ,
,
故答案为: ;
;
(3)原子电子层数越多,半径越大,电子层数相同时,核电荷数越多,半径越小,所以C、O、Na中原子半径由大到小的顺序Na>C>O,
故答案为:Na>C>O;
(4)Na2O2与H2O反应生成NaOH与O2,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)上述元素中有两种非金属元素位于同一主族,两种非金属元素为C、Si,方程式CO2+H2O+Na2SiO3=Na2CO3+H2SiO3(胶体),能证明碳非金属性更强,
故答案为:CO2+H2O+Na2SiO3=Na2CO3+H2SiO3(胶体);
(5)在25℃、101kPa下,SiH4在氧气中完全燃烧生成SiO2,反应中每转移1mole-,参加反应的SiH4为$\frac{1}{8}$mol,故1molSiH4燃烧放出的热量为190.0kJ×8=1520kJ,故该反应的热化学方程式是SiH4(g)+2O2 (g)=SiO2(s)+2H2O(l)△H=-1520.0 kJ/mol,
故答案为:SiH4(g)+2O2 (g)=SiO2(s)+2H2O(l)△H=-1520.0 kJ/mol.
点评 本题考查结构性质位置关系、常用化学用语、元素化合物性质等,难度不大,注意掌握热化学方程式的书写.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
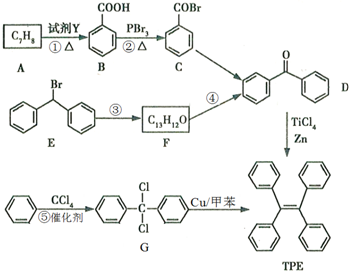
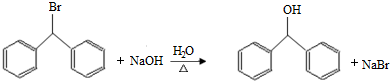 .
.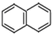 )的一元取代物;②能发生银镜反应.满足条件的W的结构简式共有4种(不考虑顺反异构).
)的一元取代物;②能发生银镜反应.满足条件的W的结构简式共有4种(不考虑顺反异构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏时,温度计水银球靠近蒸馏烧瓶的支管口处,且冷却水从冷凝管的上口通入下口流出 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 向1 mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 降低温度 | B. | 升高温度 | C. | 减小体积 | D. | 增大体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 缺乏维生素C易发夜盲症 | |
| B. | 糖尿病患者吃糖量必须限制,但淀粉类事物不必进行限制 | |
| C. | 亚硝酸钠是一种常用的发色剂,但在食品加工或餐饮业中一定要严加控制使用量 | |
| D. | 餐饮业产生的“地沟油”的主要成分是油脂,一定条件下,油脂水解可以生成高级脂肪酸和甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com