
【题目】(1)煤的利用可以是直接燃烧,也可以是先气化再燃烧 ,下面用等量的C分别按两途径进行反应
a. C(s)+O2(g) = CO2(g) △H =E1
b. C(s) +H2O(g)=CO(g)+H2 (g) △H =E2
H2(g)+![]() O2(g)=H2O(g ) △H =E3
O2(g)=H2O(g ) △H =E3
CO(s)+![]() O2(g)=CO2(g) △H =E4
O2(g)=CO2(g) △H =E4
甲同学认为:煤的气化效率高,所以b途径产生的热量高。乙同学认为,a、b途径产生的热量在理论上应该相同,你认为_____同学说法正确,理由是______________。
(2)在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)是否等于 c(M+),要看一元酸HA是强酸还是弱酸。你认为_____同学说法正确,理由是______________
【答案】乙 反应热与途径无关,只与物质的始态和终态有关(E1=E2+E3+E4) 甲 根据电荷守恒,已知c(H+)=c(OH-),所以c(A-)=c(M+)
【解析】
(1)根据盖斯定律分析解答;
(2)根据溶液呈电中性分析解答。
(1)煤气化,然后燃烧,根据盖斯定律,物质反应过程中能量变化只与物质的始态和终态有关,与反应途径无关,所以只要物质的量不变,反应物、生成物的状态不变,则反应过程的能量不变,所以a、b途径产生的热量在理论上应该相同,乙同学的认识是合理的;这可以根据热化学方程式叠加得到证实。①C(s)+O2(g) = CO2(g) △H1 =E1
②C(s)+H2O(g)=CO(g)+H2 (g) △H2=E2
③H2(g)+![]() O2(g)=H2O(g ) △H3=E3
O2(g)=H2O(g ) △H3=E3
④CO(s)+![]() O2(g)=CO2(g) △H4=E4
O2(g)=CO2(g) △H4=E4
②+③+④,整理可得C(s)+O2(g)=CO2(g),所以△H=△H2+△H3+△H4= E2+E3+E4=△H1=E1;即E1=E2+E3+E4;
(2)在任何溶液中阳离子带有的正电荷总数与阴离子带有的负电荷总数相等,所以c(M+)+c(H+)=c(OH-)+c(A-),在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性,则c(H+)=c(OH-),所以c(A-)=c(M+)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。
Ⅰ.探究一:备选药品:镁片、铝片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同学研究的实验报告:
实验步骤 | 现象 | 结论 |
①用砂纸打磨镁片和铝片; ②分别取等体积等浓度的硫酸于两支试管中; ③将镁片和铝片同时投入到试管中。 | 金属的性质越活泼, 反应速率越快 |
(1)甲同学用砂纸打磨镁片和铝片的原因是______________________________;选择H2SO4浓度为________________。
(2) 实验报告中现象为_______________________________________________。
Ⅱ.探究二:实验室经常用Na2S2O3与H2SO4的反应探究化学反应速率的影响因素,利用图1所示装置(夹持装置略去)进行实验,观察到锥形瓶底部有淡黄色浑浊。
(3)请用化学方程式表示出实验原理_________________________________,乙同学在实验过程中对产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据并绘制出图像(如图2)。
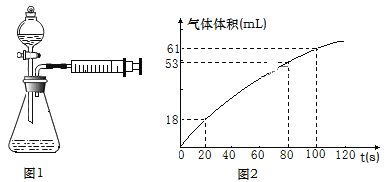
0~20s内反应速率υ1=__________mL·s-1,80~100s内反应速率υ2=__________mL·s-1。不考虑实验测量误差,分析速率差异的主要原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的CO气体和CO2气体相比较,下列叙述中正确的是
A.物质的量之比为7:11B.原子数之比为22:21
C.体积之比为1:1D.密度之比为11:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是一种短周期元索,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生右下图转化关系.其中R为10电子分子,是一种常见的无机溶剂。下列说法中不正确的是
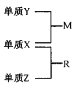
A. X元素位于周期表中第16列
B. X、Y、Z元素两两之间均能形成原子个数比为l:1的化合物
C. X、Y、Z元素形成的单质均具有强还原性
D. R的沸点高于M的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铁是有机合成的催化剂,为棕黄色固体,易潮解产生白雾,300℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,下图是甲组学生设计的制备装置。
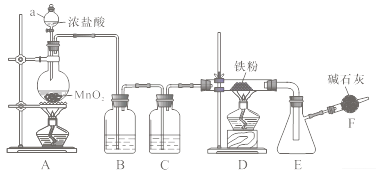
回答下列问题:
(1)仪器a的名称是________;装置B的作用是_________,C中盛装试剂是______。
(2)装置D中发生反应的化学方程式为___________________。
(3)装置D与E之间不用玻璃导气管连接,原因是_________;点燃装置D处酒精灯的时机是_______。
(4)装置F的作用是_____________。
(5)与甲组设计对比,乙组同学去掉了装置C。实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是__________,其依据是(用化学方程式表示)________,验证该猜测的实验方法是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) ![]() 2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )
2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )

A.30~40 min间该反应使用了催化剂
B.化学方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.锅炉水垢中的![]() 经饱和碳酸钠溶液浸泡可转化为
经饱和碳酸钠溶液浸泡可转化为![]()
B.常温下,在含有![]() 和
和![]() 的溶液中,
的溶液中,![]() 和
和![]() 浓度之积是个常数
浓度之积是个常数
C.当醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则溶液的导电能力一定变强
D.将浓度为![]()
![]() 的HF溶液加水不断稀释,溶液
的HF溶液加水不断稀释,溶液![]() 始终保持增大
始终保持增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图象直观地描述化学反应的进程或结果(图④纵坐标表示难溶物达到饱和时的浓度)。下列对图象描述正确的是

A.根据图①可判断可逆反应A2(g) +3B2(g)![]() 2AB3(g)的△H>0
2AB3(g)的△H>0
B.图②可表示压强对可逆反应2A(g) +2B(g)![]() 3C (g) + D(s)的影响,乙的压强大
3C (g) + D(s)的影响,乙的压强大
C.图③可表示向乙酸溶液中通入氨气至过量的过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH在4左右
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com