
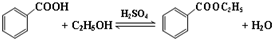
| 沸点(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 环己烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 环己烷、乙醇和水共沸物 | 62.1 |

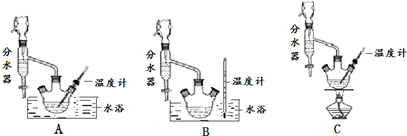
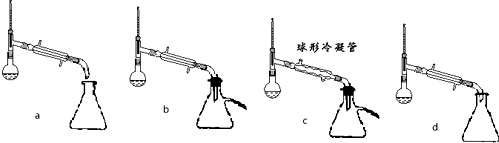
分析 (1)根据步骤②控制温度在65~70℃缓慢加热液体回流,可判断选择水浴加热的方式,要控制水浴的温度,所以温度计应测量水的温度,故选B装置,由于水-乙醇-环己烷三元共沸物,可以带出生成的水,可使酯化反应正向进行;
(2)根据反应产物可知,当反应完成时,不再产生水,分水器中下层(水层)液面不再升高,据此判断;
(3)反应物中用了苯甲酸和硫酸,所以加入碳酸钠可以中和酸;
(4)苯甲酸乙酯中溶解有少量水,用乙醚可以将其萃取出来;
(5)根据防止产物挥发到空气和冷凝效果选择装置,乙醚的沸点较低,用水浴即可将其蒸出;
(6)苯甲酸微溶于水,使用乙醇可以增大苯甲酸的溶解度,便于充分反应;苯甲酸铜冷却后会结晶析出,所以要趁热过滤;
(7)洗涤苯甲酸铜晶体时,既要除去表面可溶性杂质,又要尽可能减小苯甲酸铜晶体的溶解,且便于干燥,据此选择洗涤的试剂
解答 解:(1)根据步骤②控制温度在65~70℃缓慢加热液体回流,可判断选择水浴加热的方式,要控制水浴的温度,所以温度计应测量水的温度,故选B装置,由于水-乙醇-环己烷三元共沸物,所以环己烷在本实验中的作用是可以带出生成的水,可使酯化反应正向进行,
故答案为:B;分离出生成的水,促进酯化反应向正向进行;
(2)根据反应产物可知,当反应完成时,不再产生水,分水器中下层(水层)液面不再升高,所以反应完成的标志是分水器中下层(水层)液面不再升高,
故答案为:分水器中下层(水层)液面不再升高;
(3)反应物中用了苯甲酸和硫酸,所以加入碳酸钠可以中和酸,
故答案为:中和苯甲酸和硫酸;加入过快大量泡沫的产生可使液体溢出;
(4)苯甲酸乙酯中溶解有少量水,用乙醚可以将其萃取出来,以提高产率,
故答案为:萃取出水层中溶解的苯甲酸乙酯,提高产率;
(5)根据防止产物挥发到空气和冷凝效果选择装置b或d都可以,乙醚的沸点较低,用水浴即可将其蒸出,
故答案为:bd;水浴加热;
(6)苯甲酸微溶于水,使用乙醇可以增大苯甲酸的溶解度,便于充分反应;苯甲酸铜冷却后会结晶析出,所以要趁热过滤,
故答案为:增大苯乙酸的溶解度,便于充分反应;苯甲酸铜冷却后会结晶析出,如不趁热过滤会损失产品;
(7)洗涤苯甲酸铜晶体时,既要除去表面可溶性杂质,又要尽可能减小苯甲酸铜晶体的溶解,且便于干燥,苯甲酸铜易溶于水,难溶于乙醇,
故选C.
点评 本题考查了物质制备方案的设计,题目难度中等,明确制备原理为解答关键,试题涉及酯化反应原理、化学实验基本操作方法、化学平衡的影响因素等知识,注意掌握物质制备方案的设计及评价原则,试题充分考查了学生的分析能力、理解能力及化学实验能力.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 可用丁达尔效应区分溶液和胶体 | |
| B. | 将1.0molFeCl3全部制成胶体,其中氢氧化铁胶粒为NA个 | |
| C. | Fe(OH)3胶体的电泳实验说明了胶体粒子带有电荷 | |
| D. | 江河入海口三角洲的形成,通常与胶体的性质有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 左盘高 | B. | 右盘高 | C. | 仍保持平衡 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用如图装置,可以在室温和一个标准大气压条件下测定镁的相对原子质量.
利用如图装置,可以在室温和一个标准大气压条件下测定镁的相对原子质量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D的浓度减小了 | B. | A的转化率减小了 | ||
| C. | 物质B的质量分数增加了 | D. | a+b>c+d |
查看答案和解析>>
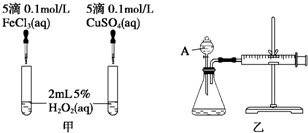
科目:高中化学 来源: 题型:实验题
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C2H4O2的有机物不一定有酸性 | |
| B. | 当物质中的化学键发生断裂时,一定发生化学变化 | |
| C. | 等质量的Al分别按a、b两种途径完全转化,途径a比途径b产生的H2多 途径a:Al$\stackrel{HCl}{→}$H2 途径b:Al$\stackrel{Fe_{2}O_{3}}{→}$Fe$\stackrel{HCl}{→}$H2 | |
| D. | 只由一种元素的阳离子与另一种元素的阴离子组成的物质不一定是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
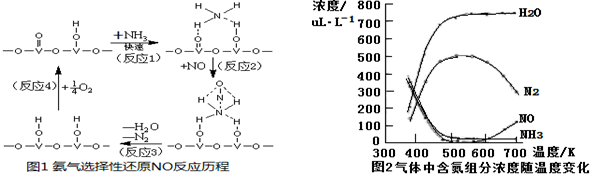
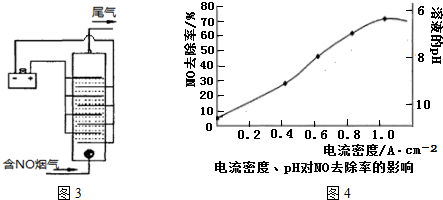
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物 的名称为:2,6-二甲基-5-乙基庚烷 的名称为:2,6-二甲基-5-乙基庚烷 | |
| B. | 丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 | |
| C. | 大气污染物氟利昂-12的化学式是CF2Cl2具有正四面体结构 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com