
| A、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、Na2O与盐酸反应:Na2O+2H+=2Na++H2O |
| C、向氢氧化钠溶液中通人过量C02:C02+OH-=HCO3- |
| D、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
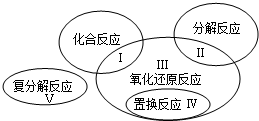 已知氧化还原反应与四种基本反应类型的关系可用如图表示,下列是有水参加或生成的几种反应:
已知氧化还原反应与四种基本反应类型的关系可用如图表示,下列是有水参加或生成的几种反应:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氢气所含原子数是2NA |
| B、5.4g水所含的分子数为0.3NA |
| C、含1mol硫酸钾的溶液中硫酸根离子数为2NA |
| D、1mol金属钠与水反应失去的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1摩尔甲醇的体积约为22.4L |
| B、1摩尔庚烷中含有的共用电子对数为23摩尔 |
| C、1摩尔氢氧根离子(OH-)与羟基(-OH)所含电子数均为10NA |
| D、2.8 g乙烯与丙烯的混合物中含总原子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶于水生成的Al(OH)3胶体,可除去水中的悬浮颗粒等杂质 |
| B、可用丁达尔现象区别Al(OH)3胶体和蔗糖溶液 |
| C、可用燃烧的方法鉴别真丝和人造丝 |
| D、构成人体蛋白质的20多种氨基酸都能通过人体自身合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20℃1mol/L稀硫酸 |
| B、30℃1mol/L稀硫酸 |
| C、20℃2mol/L稀硫酸 |
| D、30℃2mol/L稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
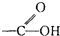 中的一0H被氨基一NH2取代所得的化合物称为酰胺.下列化合物中可以看作酰胺的是
中的一0H被氨基一NH2取代所得的化合物称为酰胺.下列化合物中可以看作酰胺的是| A、HCOONH4 |
| B、CH(NH2)3 |
| C、H2N-CH2一COOH |
| D、C0(NH2)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.7 g 金属铝所含电子数目为0.3N |
| B、16 g CH4所含原子数目NA |
| C、17 g NH3所含电子数目为NA |
| D、18 g 水所含分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com