
����Ŀ������������Ԫ��A��B��C��D��E��F��ԭ�����������������ǵ�ԭ�Ӻ�����Ӳ���֮��Ϊ13��B�Ļ���������࣬��Ŀ�Ӵ�C��D �ǿ����к�����������Ԫ�أ�D��E����Ԫ�صĵ��ʷ�Ӧ�����������ֲ�ͬ�����ӻ����FΪͬ���ڰ뾶��С��Ԫ�ء��Իش��������⣺
��1��д��D��E��1��1��ԭ�Ӹ������γɵĻ�����ĵ���ʽ��_______ ��F��ԭ�ӽṹʾ��ͼΪ_______��
��2��B��D�γɵĻ����� BD2�д��ڵĻ�ѧ��Ϊ_______ ��������ӡ����ۡ�����ͬ����A��C��F����Ԫ���γɵĻ�����CA4FΪ_______�����
��3��������ס�����A��B��D��E�е����ֻ�������ɣ��Ҽס��ҵ�ˮ��Һ���ʼ��ԣ���ס��ҷ�Ӧ�����ӷ���ʽΪ_______��
��4��A��C��D��E��ԭ�Ӱ뾶�ɴ�С��˳����_______����Ԫ�ط��ű�ʾ����
��5��Ԫ��B��F�ķǽ�����ǿ����B�ķǽ�����_______��F���ǿ���������������û�ѧ����ʽ֤����������_______��
���𰸡� ![]()
 ���� ���� OH��+HCO3���TCO32��+H2O Na��N��O��H �� Na2CO3+2HClO4�TCO2��+H2O+2NaClO4
���� ���� OH��+HCO3���TCO32��+H2O Na��N��O��H �� Na2CO3+2HClO4�TCO2��+H2O+2NaClO4
��������
�������B�γɵĻ���������࣬ȷ��BΪCԪ�أ�����C��DΪ�����к�����������Ԫ�أ���A��B��C��D��E��F��ԭ������������������CΪNԪ�أ�DΪOԪ�أ�D��E�γ����ֲ�ͬ�����ӻ������EΪNa��FΪͬ���ڰ뾶��С��Ԫ�أ�E��Fͬ���ڣ�����FΪClԪ�أ����ǵ�ԭ�Ӻ�����Ӳ���֮��Ϊ13����AΪHԪ�أ�
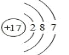
��1��NaԪ����O��ԭ�Ӹ���Ϊ1��1�γɵĻ�����ΪNa2O2�������ʽΪ![]() ��FΪClԪ�ؾ���17�����Ӻ�17�����ӣ�ԭ�ӽṹʾ��ͼΪ��
��FΪClԪ�ؾ���17�����Ӻ�17�����ӣ�ԭ�ӽṹʾ��ͼΪ��
��2��B��D�γɵĻ�����CO2�д��ڵĻ�ѧ��Ϊ���ۼ���A��C��F����Ԫ���γɵĻ�����CA4FΪNH4Cl���������Ӽ��������ӻ����
��3��������ס�����A��B��D��E�е����ֻ�������ɣ��Ҽס��ҵ�ˮ��Һ���ʼ��ԣ�����ҿ�����NaOH��NaHCO3�������䷴Ӧ�����ӷ���ʽΪ��OH-+HCO3-�TCO32-+H2O��
��4��A��C��D��E�ֱ�ΪH��N��O��Na��H�����ڱ��а뾶��С�ģ�ͬ����ԭ������Խ��뾶ԽС������N��O����ͬ���ڵ��Ӳ�Խ��뾶Խ������ԭ�Ӱ뾶Na��N�����ɴ�С��˳��Ϊ��Na��N��O��H����5��Ԫ��B��F�ķֱ�ΪC��Cl���ǽ�����C��Cl�������������Ʊ�̼�ᣬ�����������Դ���̼�ᣬ���ǽ����ԣ�Cl����C���䷴Ӧ����Ϊ��Na2CO3+2HClO4�TCO2��+H2O+2NaClO4��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ���ǣ� ��
A. KOH��Ħ��������56g
B. һ��������̼���ӵ�������������Է�������
C. ��ԭ�ӵ�Ħ����������������ԭ������
D. ������Ħ�������Կ�ÿĦ��Ϊ��λʱ����ֵ�ϵ����������ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˴�KCl��MnO2�Ļ�����л���MnO2�����в���˳����ȷ���ǣ���֪MnO2Ϊ��ɫ������ˮ�Ĺ��壩�� ��
A.�ܽ� ���� ���� ϴ��B.�ܽ� ���� ϴ�� ����
C.�ܽ� ���� ���� ����D.�ܽ� ϴ�� ���� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������۷ֱ����������Һ�У��ܷų��������ҿ��ܴ���������ǣ� ��
A.H+��Ba2+��Cl����NO3��
B.NH4+��CO3����NO3����Na+
C.NO3����K+��[Al��OH��4]����OH��
D.Na+��Ba2+��Mg2+��HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ӻ������Һ��й��ۼ����ǣ� ��
A.KOH
B.MgCl2
C.HCl
D.N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ���Ȼ���ϡ��Һ�ļס�����֧�Թ��зֱ�ͨ��SO2�����ͣ�������Թ��м����������ᣬ���Թ��м�����������������Һ��������������ȷ���ǣ� ��
A.�ס������Թܶ��а�ɫ��������
B.�ס������Թܶ�û�а�ɫ��������
C.���Թ�û�а�ɫ�������ɶ����Թ���
D.���Թ��а�ɫ�������ɶ����Թ�û��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S�ķֽⷴӦ��һ�����淴Ӧ���������뷴Ӧ���̵Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ������ ��
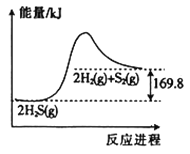
A. ����Ӧ�Ļ�ܴ����淴Ӧ�Ļ��
B. ����С��ϵ��ѹǿ����÷�Ӧ���ʱ佫����
C. �����¶�����ѧ��Ӧ���ʼӿ���H2S��ƽ��ת���ʼ�С
D. ���ܱ������г���1molH2S��ַ�Ӧ������84.9kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����1��Zn��s����1/2O2��g����ZnO��s�� ��H����348.3kJ��mol��1����
��2��2Ag��s����1/2O2��g����Ag2O(s)�� ��H����31.0kJ��mol��1��
��Zn��s����Ag2O��s����ZnO��s����2Ag��s���ġ�H����
A. ��317.3kJ��mol��1 B. ��379.3kJ��mol��1 C. ��332.8kJ��mol��1 D. ��317.3kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±����ʰ���ᡢ�Ρ���������������������˳�������ȷ���ǣ� ��
�� | �� | �� | ���������� | ���������� | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | KOH | HCl | NaCl | CaO | CO |
C | NaOH | H2CO3 | CaCl2 | CuO | SO2 |
D | NaOH | HNO3 | BaCO3 | NO | SO3 |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com