
【题目】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能___B元素的第一电离能(填“<”“>”或“=”),A、B、C三种元素电负性由小到大的顺序为_________________(用元素符号表示)。
(2)D元素原子的价电子排布式是______________。
(3)C元素的电子排布图为________________________;E3+的离子符号为________。
(4)F元素位于元素周期表的____区,其基态原子的电子排布式为______________。
(5)G元素可能的性质______。
A.其单质可作为半导体材料
B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸
【答案】> N<O<F 3s2 ![]() Fe3+ ds 1s22s22p63s23p63d104s1 或[Ar]3d104s1 A
Fe3+ ds 1s22s22p63s23p63d104s1 或[Ar]3d104s1 A
【解析】
A元素的价电子构型为nsnnpn+1,n=2,A为N元素,C元素为最活泼的非金属元素,C为F元素,则B为O元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,应为Mg元素,E元素正三价离子的3d轨道为半充满状态,则原子序数为26,为Fe元素,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,为Cu元素,G元素与A元素位于同一主族,其某种氧化物有剧毒,为As元素,以此解答该题。
A元素的价电子构型为nsnnpn+1,n=2,A为N元素,C元素为最活泼的非金属元素,C为F元素,则B为O元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,应为Mg元素,E元素正三价离子的3d轨道为半充满状态,则原子序数为26,为Fe元素,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,为Cu元素,G元素与A元素位于同一主族,其某种氧化物有剧毒,为As元素,
(1)N原子最外层为半充满状态,性质稳定,难以失去电子,第一电离能大于O元素,同周期元素从左到右元素的电负性逐渐增强,即 N<O<F,
故答案为>; N<O<F;
(2)D为Mg元素,最外层电子数为2,价电子排布式为3s2,故答案为3s2;
(3)C为F元素,电子排布图为![]() ,E3+的离子符号为 Fe3+,
,E3+的离子符号为 Fe3+,
故答案为![]() ; Fe3+;
; Fe3+;
(4)F为Cu,位于周期表ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,故答案为ds; 1s22s22p63s23p63d104s1或[Ar]3d104s1;
(5)G为As元素,与Si位于周期表对角线位置,其单质可作为半导体材料,电负性比P小,因磷酸为中强酸,则As的最高价氧化物对应的水化物是弱酸,
故答案为A。


科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 碳酸钙与足量浓硝酸反应:CaCO3+2H+![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
B. 氢氧化钠溶液与稀醋酸反应:OH-+H+![]() H2O
H2O
C. 氯化铝溶液与过量氨水反应: A13++3OH-=A1(OH)3↓
D. 钠与水反应:Na+2H2O![]() Na++2OH-+H2↑
Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取干燥氨气的装置如下图所示。下列相关叙述正确的是
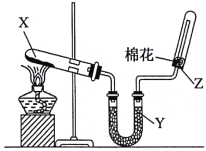
A.X处盛有的固体物质可以是NH4Cl
B.Y处盛有的固体物质可以是P2O5
C.将蘸有稀硫酸的玻璃棒靠近Z处时,有白烟产生,说明氨气已收集满
D.将湿润的红色石蕊试纸靠近Z处时,试纸变蓝,说明氨气已收集满
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家开发的一种“磷酸钒锂/石墨离子电池”在4.6V电位区电池总反应为:Li3C6+V2(PO4)3![]() 6C+Li3V2(PO4)3。下列有关说法正确的是
6C+Li3V2(PO4)3。下列有关说法正确的是
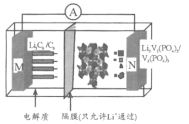
A.该电池比能量高,用Li3V2(PO4)3做负极材料
B.放电时,外电路中通过0.1 mol电子M极质量减少0.7 g
C.充电时,Li+向N极区迁移
D.充电时,N极反应为V2(PO4)3+3Li++3e-=Li3V2(PO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微粒M和N,肯定属于同族元素且化学性质相似的是( )
A.结构示意图:M为![]() ,N为
,N为![]()
B.原子核外电子排布式:M为1s22s2,N为1s2
C.M原子基态2p轨道上有一对成对电子,N原子基态3p轨道上有一对成对电子
D.M原子基态2p轨道上有1个未成对电子,N原子基态3p轨道上有1个未成对电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液HA、HB各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
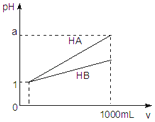
A.同浓度、同体积的HA、HB溶液分别加入过量的锌粒,产生的氢气体积后者大
B.pH相同的HA、HB溶液,物质的量浓度HA<HB
C.若1<a<4,则HA、HB都是弱酸
D.体积相同pH均为1的HA、HB溶液分别滴加同浓度的NaOH溶液至中性,前者消耗的NaOH少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是 ( )

A. 根据图①溶解度与溶液pH关系,若除去CuSO4溶液中的Fe3+可向溶液中加入适量Cu,至pH在4左右。
B. 图②可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
C. 图③表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
D. 根据图④可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的化学平衡常数K随温度升高而变小
2AB3(g)的化学平衡常数K随温度升高而变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛常温下为无色液体,熔点-23.2℃,沸点136.4℃,极易水解。在900℃时,将氯气通过钛铁矿(主要成分是FeTiO3)和炭粉的混合物可反应生成四氯化钛和氯化铁(熔点306℃,沸点315℃),同时产生一种有毒气体。现制取并收集四氯化钛的装置如图所示(夹持装置略去)。
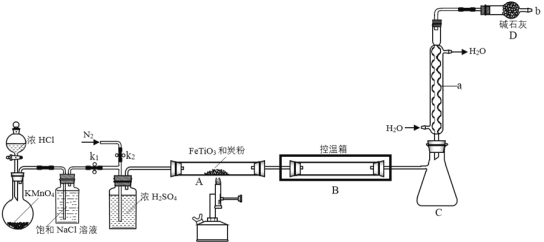
回答下列问题:
(1)仪器a的名称是____。组装好仪器,没加试剂反应前,应该进行的操作是_____。
(2)反应开始前,先将钛铁矿粉碎,并与稍过量的炭粉混合均匀,制成多孔状固体混合物,目的是______________。
(3)实验中需通入N2两次,第二次通N2的作用是_________。
(4)900℃时,A装置中发生反应的化学方程式为__________。
(5)B装置中控温箱温度在150~200℃,目的是___________。
(6)装置b处存在的缺点是________________。
(7)产物TiCl4在热潮湿空气中“发烟”生成TiO2xH2O,反应方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)具有明显现象的官能团特征反应常被用来鉴定化合物。欲区分CH3CH2OH和CH3CHO,应选用__;欲区分![]() 和
和![]() ,应用__;等浓度的下列稀溶液中①乙酸 ②碳酸 ③乙醇 ④甲酸,它们的pH由小到大排列顺序是__。
,应用__;等浓度的下列稀溶液中①乙酸 ②碳酸 ③乙醇 ④甲酸,它们的pH由小到大排列顺序是__。
(2)对羟基肉桂酸是一种强效的导电材料,近年来在液晶显示器工业中近年来研究广泛。其结构简式如图所示:
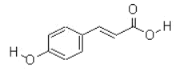
该有机物分子式为__,具有的官能团名称分别是__。
该有机物能发生的反应类型是(填写代号)__。
A.酯化反应 B.消去反应 C.加成反应 D.水解反应
(3)写出下列反应的化学方程式(有机物用结构简式表示):
用甲苯制TNT:__;
乙醛与新制的氢氧化铜悬浊液的反应:___;
1溴丙烷和KOH乙醇溶液反应:__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com