
| A. | 通式相同的两种有机物按不同比例混合时,只要总质量一定,完全燃烧的耗氧量就一定 | |
| B. | 除去甲烷中的乙烯可用溴水或酸性高锰酸钾溶液 | |
| C. | 糖类、油脂、蛋白质都会在一定条件下水解 | |
| D. | 戊烷有3种同分异构体,而一氯戊烷有8种同分异构体 |
分析 A、通式相同不一定最简式相同;
B、乙烯可和酸性高锰酸钾溶液发生氧化还原反应,氧化产物为二氧化碳气体;
C、糖类分为单糖、二糖和多糖,根据糖的分类分析解答;
D、氯代烃在组成形式上可以看作氯原子取代烷烃上的氢原子,所以戊烷基有几种一氯代烃的同分异构体就有几种.
解答 解:A、甲烷和乙烷通式相同,但最简式不同,当总质量一定,两者的比例不同,完全燃烧的耗氧量就不同,故A错误;
B、除杂不能产生新的杂质,乙烯和酸性高锰酸钾溶液发生氧化还原反应生成二氧化碳气体,所以只能用溴水除去甲烷中的乙烯,故B错误;
C、单糖不能水解,而油脂、蛋白质都会在一定条件下水解,故C错误;
D、氯代烃在组成形式上可以看作氯原子取代烷烃上的氢原子,所以戊烷基有几种一氯代烃的同分异构体就有几种.
戊烷有几种氢原子就有几种戊烷基,戊烷的三种同分异构体CH3CH2CH2CH2CH3、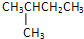 、
、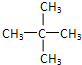 分别有3种、4种、1种氢原子,所以戊烷共能形成8种戊烷基,所以戊烷的一氯代物的同分异构体有8种,故D正确;
分别有3种、4种、1种氢原子,所以戊烷共能形成8种戊烷基,所以戊烷的一氯代物的同分异构体有8种,故D正确;
故选D.
点评 本题考查有机物的燃烧、除杂和有机中的水解反应,以及异构体的判断,D选项可以通过戊烷的同分异构体数目推断属于氯代烃的同分异构体的数目,难度不大,注意烷基数目的寻找.


科目:高中化学 来源: 题型:选择题
| A. | HA为强酸 | B. | 该混合液pH=7 | ||
| C. | X表示HA,Y表示OH,Z表示H+ | D. | 该混合溶液中:c(A-)+c(Y)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol•L-1碳酸钠溶液中的阴离子总数为0.1NA | |
| B. | 将400mL1mol/L的HNO3溶液与7gFe粉充分反应,电子转移数为0.375NA | |
| C. | 标准状况下,14g氦气中共用电子对的数目为1.5NA | |
| D. | 已知反应N2(g)+3H2(g)?2NH3(g)△H=-91.8kJ/mol的转化率为30%,当放出91.8kJ热量时,生成氨分子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>②>③>① | B. | ①>②>③>④ | C. | ①>②>④>③ | D. | ①>③>②>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 molCaC2晶体中含有的离子总数为3NA | |
| B. | 常温常压下,3g-CH3中含有的电子数为1.8NA | |
| C. | NA个HCl分子与22.4LH2和Cl2的混合气体所含有的原子数均为2NA | |
| D. | 80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.48 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
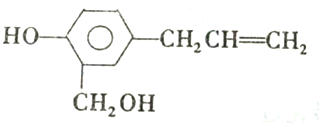 对该物质的性质判断正确的是( )
对该物质的性质判断正确的是( )| A. | 等量A分别与Na和NaOH反应消耗二者的物质的量相同 | |
| B. | 1 mol A 可与2 mol Br2发生取代反应 | |
| C. | A与Na2CO3反应可放出CO2 | |
| D. | 1 mol A 可与4 mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤 | 实验方案 | 实验现象(描述最后的) | 离子方程式 |
| ① | 先向试管中加入溴化钠溶液2ml,再加入4-5滴新制氯水,振荡后分两份,取一份又加入CCl4,振荡、静置 | 上层为浅黄色(或无色),下层为橙色 | Cl2+2Br-=Br2+2Cl- |
| ② | 取少量KI溶液于试管,加入几滴步骤①留下的另一份溶液,振荡,又加入CCl4,振荡、静置 | 上层为浅黄色(或无色),下层为紫红色 | Br2+2I-=I2+2Br- |
| 结论 | 氧化性:Cl2>Br2>I2(非金属性:Cl>Br>I) | ||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
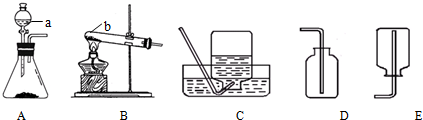
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com