
| A. | 氧化性(酸性溶液):PbO2>Fe3+>S | |
| B. | 还原性(碱性溶液):Fe(OH)2>KCl>Cl2 | |
| C. | 酸性(水溶液):H2S>H2SO4>H2SeO4>HN3 | |
| D. | 热稳定性:CaCO3>FeCO3>Ag2CO3 |
分析 A、PbO2的氧化性较强,强于高锰酸根离子,铁离子的氧化性强于单质硫,据此回答;
B、根据物质中对应元素的化合价判断还原性的强弱;
C、氢硫酸是弱酸,硫酸是强酸;
D、根据物质受热是否容易分解来判断其热稳定性.
解答 解:A、根据所学知识整理,得到:PbO2的氧化性较强,强于高锰酸根离子,铁离子的氧化性强于单质硫,所以氧化性(酸性溶液):PbO2>Fe3+>S,故A正确;
B、Fe(OH)2中亚铁离子很容易被氧气氧化,还原性强,KCl中的氯离子具有较弱的还原性,Cl2表现为较强的氧化性,即还原性(碱性溶液):Fe(OH)2>KCl>Cl2,故B正确;
C、氢硫酸是弱酸,硫酸是强酸,酸性顺序是:H2S<H2SO4;故C错误;
D、碳酸钙高温下会分解为氧化钙和二氧化碳,FeCO3、Ag2CO3的热稳定性逐渐减弱,稳定性:CaCO3>FeCO3>Ag2CO3,故D正确,
故选C.
点评 本题考查物质的性质比较知识,主要是学生根据自己已学知识来进行归纳总结,得到结论即可.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 用HR做导电实验,灯泡很暗 | |
| B. | 0.1mol•L-1HR溶液稀释到100倍时,溶液的pH值为3 | |
| C. | 20mL0.1mol•L-1HR恰好中和20mL0.1mol•L-1NaOH溶液 | |
| D. | 0.1mol•L-1NH4R溶液的pH等于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①⑤ | B. | ①②③ | C. | 全部 | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
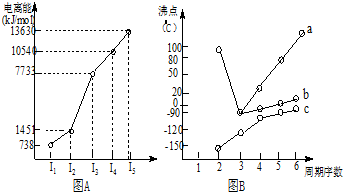
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 | 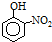 | 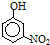 | 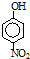 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制备乙烯时,产生的气体使溴水褪色,能证明有乙烯生成 | |
| B. | 加热NaOH和少量溴乙烷的混合液后滴加硝酸银,可生成浅黄色沉淀 | |
| C. | 制取硝基苯时,试管中先加入浓H2SO4,再逐滴滴入浓HNO3和苯,振荡混合均匀后,保持55℃水浴加热 | |
| D. | 除去溴苯中的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al原子的失电子能力逐渐减弱 | |
| B. | Si、P、S元素的最高正化合价依次降低 | |
| C. | C、N、O的原子半径依次减小 | |
| D. | Cl、Br、I的气态氢化物的稳态性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 和过量的 NaOH 溶液充分反应并加热,可生成标准状况下的 NH3 4.48L | |
| B. | 通入 H2S 气体,发生反应的离子方程式为:H2S+Fe2+=FeS↓+2H+ | |
| C. | Ca2+、ClO-、Cl-、Cu2+能在该溶液中大量共存 | |
| D. | Cl-、H+、I-、Na+不能在该溶液中大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com