
分析 (1)根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态来解答;
(2)A、化石燃料属于不可再生的能源
B、甲烷燃烧是放热反应,结合能量守恒分析判断物质的能量变化;
C、液态水变化为气态水吸热,反应放出热量数值减小,焓变为负值比较大小.
解答 解:(1)16g即1molCH4在氧气中燃烧生成CO2和液态水,放出889kJ热量,则热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.31KJ/mol,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.31KJ/mol;
(2)A、天然气属于化石燃料,属于不可再生的能源,故A正确;
B、甲烷燃烧是放热反应,结合能量守恒分析,反应物能量高于生成物,故B正确;
C、液态水变化为气态水吸热,反应放出热量数值减小,焓变为负值比较大小,25℃、101kPa 时,16g的CH4物质的量为=$\frac{16g}{16g/mol}$=1mol,完全燃烧生成气态水时放出的热量小于890.31kJ,故C错误;
故答案为:AB.
点评 本题主要考查了热化学方程式的书写,题目难度不大,注意物质的量与热量成正比是解题的关键.注意标注物质聚集状态和对应焓变.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质在实验室一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题:
A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质在实验室一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题:| … | E | A | B | ||
| C | … | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | NH3、NO2、N2 | B. | NH3、NO、CO2 | C. | HCl、NO2、CO2 | D. | NO、CO2、N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加A2 的浓度,有利于该反应平衡逆向移动 | |
| B. | 升高温度有利于该反应平衡正向移动 | |
| C. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| D. | 增大压强有利于该反应平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

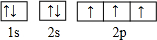 ,这样排布遵循了构造原理、泡利原理和洪特规则.
,这样排布遵循了构造原理、泡利原理和洪特规则.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{24n}{m-n}$ | B. | $\frac{n}{24(m-n)}$ | C. | $\frac{m-n}{8}$ | D. | $\frac{2(m-n)}{3n}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和石油的分馏均属物理变化 | |
| B. | 为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂 | |
| C. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| D. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com