
| A������Һ��ϣ�AgCl��AgI������ |
| B����AgI��Һ����AgNO3��c��Ag+������KSp��AgI��Ҳ���� |
| C����AgNO3������AgCl��AgI���ɳ���������AgClΪ�� |
| D����ȡ0.1435��AgCl�������100mLˮ����������仯����c��Cl-��Ϊ0.01mol/L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
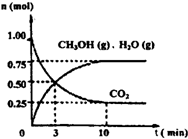 ��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���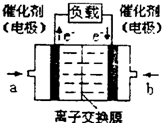
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����ʵ | ���ۻ���� | �� | ��40g NaOH����1L����ˮ�� | �� ��Һ�����ʵ���������Ϊ3.84%�������ʵ���Ũ��Ϊ1molL-1 | �� | ��ʢ��1mL 0.1mol?L-1AgNO3��Һ���Թ��еμ�0.1molL-1NaCl��Һ���������г������ɣ��������е�0.1molL-1 KI��Һ����ɫ����ת��Ϊ��ɫ������ |
������ Ksp��AgCl����Ksp��AgI�� |
�� | ij��NaX��ҺpH��7 | ��HXΪ���� | �� | ��ij��Һ�м���2��KSCN��Һ����Һ���Ժ�ɫ��������Һ�м��뼸�����Ƶ���ˮ����Һ��Ϊ��ɫ | ˵����Һ��һ������Fe2+ | �� | ��ʢ��Ũ������Թ��зֱ����AlƬ�� CuƬ��ǰ��û�����������߷�Ӧ���ң�������������ɫ���� |
��ԭ��Al��Cu | �� | BaSO4��ˮ��Һ�����Ժܲ� | BaSO4��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ��������У������ѧ����ĩ���ԣ����ۣ���ѧ���� ���ͣ�ѡ����
��������ʵ���ó��Ľ��ۻ�����Ľ�����ȷ���ǣ� ��
|
|
ʵ����ʵ |
���ۻ���� |
|
�� |
��40 g NaOH����1 L����ˮ�� |
�� ��Һ�����ʵ���������Ϊ3.84%�������ʵ���Ũ��Ϊ1molL-1 |
|
�� |
��ʢ��1mL 0.1mol��L-1 AgNO3��Һ���Թ��еμ�0.1molL-1 NaCl��Һ���������г������ɣ��������е�0.1molL-1 KI��Һ����ɫ����ת��Ϊ��ɫ������ |
������ Ksp��AgCl��< Ksp��AgI�� |
|
�� |
ij��NaX��ҺpH > 7 |
��HX���� |
|
�� |
��ij��Һ�м���2��KSCN��Һ����Һ���Ժ�ɫ��������Һ�м��뼸�����Ƶ���ˮ����Һ��Ϊ��ɫ |
˵����Һ��һ������Fe2+ |
|
�� |
��ʢ��Ũ������Թ��зֱ����AlƬ�� CuƬ��ǰ��û�����������߷�Ӧ���ң�������������ɫ���� |
��ԭ��Al < Cu |
|
�� |
BaSO4��ˮ��Һ�����Ժܲ� |
BaSO4��������� |
A���٢ܢ� B���ۢܢ� C���ۢ� D���ڢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com