
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �ܢݢ� | D�� | �٢� |
���� ��17.6g�������ʵ���Ϊ0.4mol��ÿĦ�������к��й��ۼ�10mol��
��C3H6��C4H8�����ʽΪCH2���������ʽ�����������к��е�̼ԭ������
�۲�һ�����ڱ�״���£�
������n=$\frac{m}{M}$�������ʵ������ټ���������
���������Ƶ�������������ӣ�����ˮ�ĵ��룻
�����������������ļ����壮
��� �⣺��17.6g�������ʵ���Ϊ$\frac{17.6g}{44g/mol}$=0.4mol��ÿĦ�������к��й��ۼ�10mol������0��4mol���麬���ۼ�Ϊ0.4mol��10=4mol����4NA���ʢ���ȷ��
�ڳ����£�21g C3H6��C4H8�Ļ�����к������ʽCH2�����ʵ���Ϊ$\frac{21g}{14g/mol}$=1.5mol���ʺ��е�̼ԭ����Ϊ1.5mol����1.5NA���ʢ���ȷ��
�۲�һ���ڱ�״���£�2.24L H2��һ����0.1mol���ʢ۴���
������2gD216O�����ʵ���=$\frac{2g}{20g/mol}$=0.1mol���������е�������Ϊ0.1mol��10=1mol����NA�������е�������Ϊ0.1mol��10=1mol����NA�������еĵ�����Ϊ0.1mol��10=1mol����NA�����ʢ���ȷ��
�ݳ����£�pH=13��NaOH��Һ�У����е�OH-��ĿΪ0.1mol����0.1NA���������Ƶ�������������ӣ�����ˮ�ĵ��룬����ˮ�����OH-������ĿԶС��0.1NA���ʢݴ���
�����������������ļ����壬��100mL0.1mol•L-1��FeCl3��Һ�����ˮ�п��Ƶ�Fe��OH��3����С��0.01NA���ʢ���
��˵������ȷ���ǣ��٢ڢܣ�
��ѡA��
���� ���⿼�鰢��٤��������Ӧ�ü����㣬�Ѷ��еȣ�Ҫע����������Ħ�������ʹ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �ҿ� | C�� | ��� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 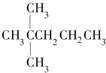 | B�� | CH3CH2CH2CH2CH3 | C�� | 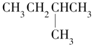 | D�� | 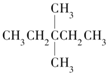 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| A | ���������Ӳ㣬K��M�������֮�͵���L������� |
| B | �������н�������ǿ |
| C | �����µ���Ϊ˫ԭ�ӷ��ӣ��⻯���ˮ��Һ�ʼ��� |
| D | Ԫ�����������+7�� |
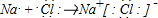 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
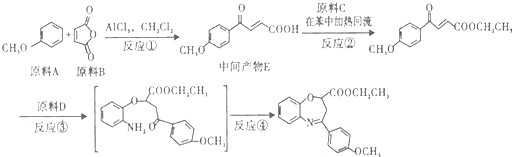
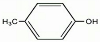 ��д����ṹ��ʽ����
��д����ṹ��ʽ����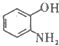 ��
��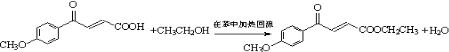 ��
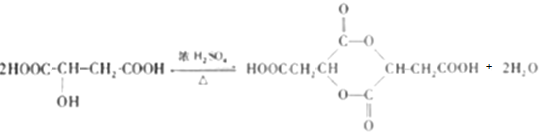
��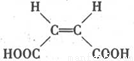 ���������������Ծ����б仯�ֱ�õ�ƻ���ᣨ
���������������Ծ����б仯�ֱ�õ�ƻ���ᣨ ���;ۺ���Q��
���;ۺ���Q��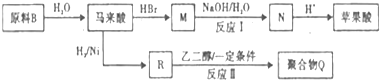
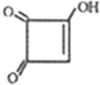 ��
��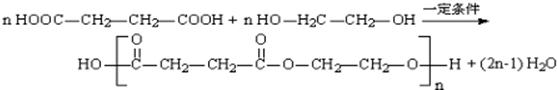 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
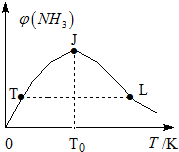 ������������Դ����Ҫ����ԭ�ϣ�
������������Դ����Ҫ����ԭ�ϣ�| ������� | ��ʼʱ�����ʵ����ʵ���/mol | ƽ��ʱ��Ӧ�е������仯 | ||
| H2 | N2 | NH3 | ||
| �� | 3n | n | 0 | �ų�����a kJ |
| �� | 3n | 2n | 0 | �ų�����b kJ |
| �� | 6n | 2n | 0 | �ų�����c kJ |
| ʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | �� |
| NH3/mol | 2 | 1.0 | 0.5 | 0.25 | 0.24 | 0.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����������������������ڲ�ͬ��ʵ�������½��з�Ӧ������ڲ�ͬʱ�䣨t���ڲ������������V����������ͼ��ʾ������ͼʾ����ʵ������������˵����һ������ȷ���ǣ�������
����������������������ڲ�ͬ��ʵ�������½��з�Ӧ������ڲ�ͬʱ�䣨t���ڲ������������V����������ͼ��ʾ������ͼʾ����ʵ������������˵����һ������ȷ���ǣ������� | ��� | ��Ӧ���� | c��HCl��/mol•L-1 | ��Ӧ�¶�/�� | ����״̬ |
| 1 | a | 30 | ��ĩ״ | |
| 2 | b | 30 | ��ĩ״ | |
| 3 | c | 2.5 | ��״ | |
| 4 | d | 2.5 | 30 | ��״ |
| A�� | ��4��ʵ��ķ�Ӧ�������� | |
| B�� | ��1��ʵ���������Ũ�ȴ���2.5 mol•L-1 | |
| C�� | ��2��ʵ���������Ũ�ȵ���2.5 mol•L-1 | |
| D�� | ��3��ʵ��ķ�Ӧ�¶ȵ���30�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԭ�������ͺ�������� | B�� | ���Ӳ��������������� | ||
| C�� | ���ԭ������������������ | D�� | ���Ӳ����ʹ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com