
【题目】用式量为43的烷基取代甲苯苯环上的一个氢原子最多可得到取代产物( )
A.3种
B.4种
C.5种
D.6种
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3﹣己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请同学们根据官能团的不同对下列有机物进行分类.把正确答案填写在题中的横线上①CH3CH2OH② ![]() ③CH3CH2Br④
③CH3CH2Br④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]() ⑦
⑦ ![]() ⑧
⑧ ![]() ⑨
⑨ ![]() ⑩
⑩ ![]()
(1)芳香烃:;
(2)卤代烃:;
(3)醇:;
(4)酚:;
(5)醛:;
(6)酮:;
(7)羧酸:;
(8)酯: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示某反应进行时,有酶参与和无酶参与的能量变化,则下列叙述正确的是( )
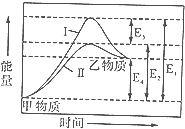
A.此反应为放能反应
B.曲线Ⅰ表示有酶参与
C.E1为反应前后能量的变化
D.酶参与反应时,所降低的活化能为E3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为短周期元素,原子序数依次递增.A元素原子核内无中子.B元素原子核最外层电子数是次外层电子数的2倍.C元素是地壳中含量最多的元素.D是短周期元素中金属性最强的元素.E与F的位置相邻,F的最高价氧化物的水化物为最强酸.
(1)推断B在元素周期表中的位置:第周期,第族.
(2)写出F的电子排布式: .
(3)C、D可形成淡黄色的粉末,其电子式为 .
(4)写出A与C形成的10电子微粒的化学式:、、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1L0.1mol/L Na2S2O3溶液与一定量的pH=2的硫酸溶液混合,放出VL气体.NA代表阿伏伽德罗常数的值,下列说法正确的足( )
A.pH=2的硫酸溶液含有H+数目为0.01NA
B.该反应释放SO2分子数目为 ![]() NA
NA
C.反应中每摩尔Na2S2O3转移的电子数目为4NA
D.若98gH2SO4溶于水完全电离,其断裂的共价键数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 2.24L甲烷气体中碳氢键的数目为0.4NA
B. lmolSO2与足量的O2反应,转移的电子数为2NA
C. 1 mol·L-1CH3COOH 与1 mol·L-1CH3COONa 溶液等体积混合,溶液中CH3COOH 和CH3COO-的总数为2NA
D. 7.8g乙炔与苯的混合物完全燃烧所消耗的O2分子数为0.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中能大量共存的离子组是( )
A. Ba2+、H+、HCO3-、Cl- B. Cu2+、OH-、NH4+、Cl-
C. Ag+、NO3-、Cl-、H+ D. Na+、NO3-、SO42-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的流程如下:
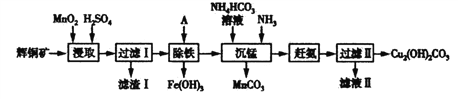
(1)辉铜矿中铜元素的价态为_________________。
(2)滤渣Ⅰ的成分除了不溶性矿渣外,还有S、__________、______________,写出“浸取”过程中生成S 的离子方程式_______________________。
(3)也可用FeCl3代替MnO2作浸取剂。若向FeCl3浸取液中加入CuCl2 ,能加快铜元素的浸取速率,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S;②____________。
(4)“沉锰”时发生的反应的离子方程式为____________________。
(5)滤液Ⅱ经结晶得到的盐主要是____________(填化学式,下同),流程中可循环的物质是_________________。
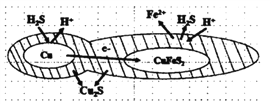
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见下图,转化时负极的电极 反应式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com