
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①C(s)+O2(g)===CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
A. ① B. ④ C. ②③④ D. ①②③
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关合金的说法错误的是
A. 青铜是我国使用最早的合金 B. 钢是用量最大、用途最广的合金
C. 合金的硬度一般高于各成分金属 D. 合金的熔点一般高于各成分金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关。下列说法错误的是
A. 纤维素是多糖,可以作人类的营养物质
B. 利用高纯度单质硅可以制成太阳能光伏电池
C. 制作宇宙飞船的玻璃纤维和玻璃的成分相同
D. C1O2可用作自来水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高铁酸钠(Na2FeO4)是一种绿色消毒净水剂,只在碱性环境中稳定存在。下列是通过次氧酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.制备高铁酸钠(Na2FeO4)
(1)制备NaClO溶液
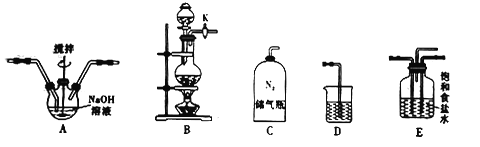
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
①如何检查装置B的气密性?____________________________________________。
②实验室制取Cl2的化学方程式是_______________________,利用如图所给的装置组装成制备NaClO的正确连接顺序是![]() ________(填字母),其中装置E的作用是________(填序号)。
________(填字母),其中装置E的作用是________(填序号)。
a.混合气体 b.除去氯气中的氯化氢 c.干燥气体 d.观察气体的通入速率
③为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________________。
(2)制备Na2FeO4:将Fe(NO3)2溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是___________________________________。
II.高铁酸钠(Na2FeO4)具有强氧化性,某实验小组的同学对于高铁酸钠消毒后铁元素的存在形式展开如下探究:
【提出猜想】:猜想1:全部为Fe2+ 猜想2:全部为Fe3+ 猜想3: Fe2+和Fe3+都有
【设计实验】:
(1)证明溶液中只含有Fe2+的实验操作是_________________________________。
(2)某实验小组将消毒后的溶液分在两支试管中,进行如下实验:
步骤一:向试管1中加入K3[Fe(CN)6]溶液,现象是__________,所以溶液中不存在Fe2+;
步骤二:向试管2中滴入KSCN溶液,溶液变成血红色,所以溶液中存在Fe3+。
【实验结论】:高铁酸钠消毒后溶液中只存在Fe3+。
(3)小明同学认为上述实验结论不够严谨,原因是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组验证乙醇的还原性,装置如下:

(1)乙醇被氧化的产物为______________,1mol乙醇失去___________mol电子。
(2)通入乙醇反应,试管A的现象是___________;反应结束后,如果对试管B进行加热,将会出现的现象是_____________________。
(3)研究小组发现,反应后期有不溶于水的气体出现,收集该气体证明是H2,为了进一步研究设计了如下装置(部分加热仪器已省略):

①C装置盛有的物质是_____________,先加热____________(填装置代号),赶走装置内的空气。
② E收集液体产物,甲认为是乙酸,乙认为还是乙醛,请你判断谁的推测更合理,并说明理由:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是

A. 用装置甲验证HCl气体易溶于水
B. 用装置乙验证SO2具有漂白性
C. 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D. 用装置丁检验NH4Cl分解产生的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关。下列说法正确的是
A. 阻燃剂Al(OH)3受热分解时放出能量
B. 蚕丝、涤纶、棉花的主要成分均为蛋白质
C. 油脂在长期贮存过程中与微生物、酶和空气中的氧气作用会发生酸败
D. 硅太阳能电池与铜锌原电池工作时均由化学能转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4 molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3 molL-1s-1
②物质 B的体积分数是40%
③2 s 时物质 A 的转化率为30%
④2 s 时物质 B 的浓度为 1.0 molL-1
其中正确的是
A. ①④ B. ②③ C. ①③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com