
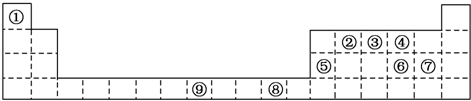
分析 由元素在周期表中位置,可知①为H、②为C、③为N、④为O、⑤为Al、⑥为S、⑦为Cl、⑧为Cu、⑨为Fe.
(1)d区元素包含周期表中3-10列元素;元素⑧位于第四周IB族;
(2)N和Cl形成的常见化合物有NCl3、NCl5,均为分子晶体;由于周期表中同周期元素从左到右非金属性逐渐增强,电负性也逐渐增大,非金属性越强,气态氢化物越稳定;
(3)s能级最多容纳2个电子,且p能级容纳电子,故n=2,则该元素为N元素,氨气和水都是极性分子,相似相溶原理,又由于氨分子与水分子间可形成氢键;
(4)C、N形成的化合物为C3N4,由其超硬,耐高温等性质,可判断该化合物属于原子晶体,由于C-N键比C-C键短,C-N键键能更大,其熔点更高;
(5)Al的氧化物为Al2O3,S的最高价氧化物的水化物为H2SO4,二者反应生成硫酸铝与水.
解答 解:由元素在周期表中位置,可知①为H、②为C、③为N、④为O、⑤为Al、⑥为S、⑦为Cl、⑧为Cu、⑨为Fe.
(1)属于d区的是Fe,为⑨号元素,⑧为Cu元素,位于第四周IB族,Cu的外围电子排布为3d104s1,
故答案为:Fe;3d104s1;
(2)N和Cl形成的常见化合物有NCl3、NCl5,均为分子晶体;由于周期表中同周期元素从左到右非金属性逐渐增强,电负性也逐渐增大,即C<N<O,非金属性越强,气态氢化物越稳定,故H2O比NH3、CH4稳定,
故答案为:分子晶体;O>N>C;同周期元素从左到右的非金属性逐渐增强;H2O;
(3)s能级最多容纳2个电子,且p能级容纳电子,故n=2,则该元素为N元素,即为③号元素,氨气和水都是极性分子,根据相似相溶原理可知NH3易溶于水,又由于氨分子与水分子间可形成氢键,使NH3更易溶于水,
故答案为:③;氨气和水都是极性分子,氨气和水分子间可以形成分子间氢键;
(4)C、N形成的化合物为C3N4,由其超硬,耐高温等性质,可判断该化合物属于原子晶体,由于C-N键比C-C键短,C-N键键能更大,C3N4熔点更高,
故答案为:C3N4;高;
(5)Al的氧化物为Al2O3,S的最高价氧化物的水化物为H2SO4,二者反应的方程式为:Al2O3+3H2SO4═Al2(SO4)3+3H2O,
故答案为:Al2O3+3H2SO4═Al2(SO4)3+3H2O.
点评 本题考查元素周期表与元素周期律、分子结构与性质、晶体类型与性质等,需要学生熟练掌握元素周期表的结构,侧重考查学生对知识的迁移应用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 明矾能净水:Al3++3H2O?Al(OH)3+3H+ | |
| B. | 醋酸溶液显酸性:CH3COOH=CH3COO-+H+ | |
| C. | NaHCO3溶液显碱性:HCO3-+H2O?CO32-+OH- | |
| D. | Fe(OH)3胶体的制备:Fe3++3H2O=Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化硼是原子晶体 | |
| B. | 熔化时,氯化硼能导电 | |
| C. | 氯化硼是一种离子晶体 | |
| D. | 水解方程式:BCl3+3H2O?H3BO3+3HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m+n+2}{w}$mol | B. | $\frac{m-n+2}{m}$ mol | C. | $\frac{m+n-2}{m}$ mol | D. | $\frac{W(m-n-2)}{m}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:O<S<Na | |
| B. | 碱性强弱:LiOH>KOH>CsOH | |
| C. | 还原性:HCl>HBr>HI | |
| D. | 热稳定性:H2O<NH3<SiH4的依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 测定时刻/s | t1 | t2 | t3 | t4 |
| c(A)/(mol•L-1) | 6 | 3 | 2 | 2 |
| c(B)/(mol•L-1) | 5 | 3.5 | 3 | 3 |
| c(C)/(mol•L-1) | 1 | 2.5 | 3 | 3 |
| A. | 在t3时刻反应已经停止 | |
| B. | A的转化率比B的转化率高 | |
| C. | t1至t2时刻该反应的速率为3mol•L-1•s-1 | |
| D. | 该反应的化学方程式为2A(g)+B(g)?C(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2为0.4 mol/L | B. | SO2为0.3 mol/L、SO3为0.3 mol/L | ||
| C. | SO2为0.25 mol/L | D. | O2为0.05 mol/L、SO3为0.1 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com