
 ��
�� ����������ʽ�ܼӿ췴Ӧ���ʵ�ԭ���ǵ������������˫�����ṹ�����ı䣮
����������ʽ�ܼӿ췴Ӧ���ʵ�ԭ���ǵ������������˫�����ṹ�����ı䣮| X�������� | N-H���� | N-N���� | H-N-H���� |
| ���� | 101.9pm | 339.0pm | 107�� |
���� ��1��N2���ӽṹʽΪN��N����ԭ�ӹ�����ص���ʽ�IJ�ͬ���ڵĹ��ۼ������ЦҼ����м���N-N����Ϊ�Ҽ�����N��N������һ���Ҽ��������м���
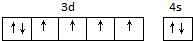
��2��Fe����26��Ԫ�أ����ݹ���ԭ����д�����Ų�ͼ��
��3����������ʽʹ������������˵���˫�������ܼ�С����Ӧ���ʼӿ죻
��4�����ݼ۲���ӶԻ�������ȷ�����ռ乹�ͺ�����ԭ���ӻ���ʽ���жϣ�������������غϵķ����ǷǼ��Է��ӣ�����������IJ��غϵ��Ǽ��Է��ӣ�
��5����̬���������������������ݾ�̯�����㣻
��6�����ݾ�����ܶ�$��=\frac{m}{V}$���㣮
��� �⣺��1��N2���ӽṹʽΪN��N����ԭ�ӹ�����ص���ʽ�IJ�ͬ���ڵĹ��ۼ������ЦҼ����м�������N-N����193kJ•mol-1��N��N����946kJ•mol-1�����Ԧм����ȶ���
�ʴ�Ϊ���Ҽ����м����м���
��2��Fe����26��Ԫ�أ���̬��ԭ�Ӽ۵����Ų�ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3���������������˫�����ṹ�����ı䣬ʹ�ü��ܼ�С���ʼӿ췴Ӧ���ʣ��ʴ�Ϊ���������������˫�����ṹ�����ı䣻
��4�������е�ԭ�Ӻ���3���Ҽ���1���µ��Ӷԣ�������۲���ӶԸ�����4���÷������������νṹ������sp3�ӻ���������������������IJ��غϣ������Ǽ��Է��ӣ��ʴ�Ϊ��������sp3�����ԣ�
��5����̬�����������������������ӵ���λ��Ϊ3��$\frac{1}{2}$��8=12���ʴ�Ϊ��12��
��6����̬������������������һ�������к��а����ӵ���ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��N-N����Ϊ339.0pm=3.39��10-8cm�����������V=��$\frac{\sqrt{2}}{2}$��2��3.39��10-8cm��3���ʾ����ܶ�$��=\frac{m}{V}$=�ʴ�$\frac{\frac{17g/mol}{6.02��1{0}^{23}mo{l}^{-1}}��4}{��\frac{\sqrt{2}}{2}��2��3.39��1{0}^{-8}cm��^{3}}$��
��$\frac{\frac{17g/mol}{6.02��1{0}^{23}mo{l}^{-1}}��4}{��\frac{\sqrt{2}}{2}��2��3.39��1{0}^{-8}cm��^{3}}$��
���� ���⿼����ԭ�Ӻ�������Ų�ͼ����ѧ�������ӿռ乹�͡���ѧ��Ӧ���ʵ�Ӱ�����ء������ļ���ȣ��Ѷ��еȣ���Ҫ�ۺ�Ӧ��֪ʶ��������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Σ��Ʒ������������з��������ơ�þ�Ż�ʱ��Ӧ��������ĭ�������� | |
| B�� | ����������Һ�IJ�������2 mL 2%����������Һ����μ���2%�İ�ˮ�����Թܣ�ֱ�������ij���ǡ����ȫ�ܽ� | |
| C�� | ����230mL 0.1mol•L-1��FeCl3��Һ����ȡһ��������FeCl3�������ձ����������������У����������º���ת����250mL����ƿ�н������� | |
| D�� | ȡ������������茶���������ˮ�ܽ⣬��������10%��NaOH��Һ�����ȣ�����ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����壬˵�������к���NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | 0.1032mol/L HCl��Һ���/mL | ����NaOH��Һ���/mL |
| 1 | 27.83 | 25.00 |
| 2 | 26.53 | 25.00 |
| 3 | 27.85 | 25.00 |
| ��ѧʽ | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| ��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ | ��ɫ |
| Ksp | 1.8��10-10 | 5.0��10-13 | 8.3��10-17 | 2.0��10-48 | 1.8��10-10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͨ��ˮ��Cl2+H2O�T2H++Cl-+ClO- | |
| B�� | ���Ƽ���ˮ��S2-+2H2O�TH2S+2OH- | |
| C�� | ���������ˮ��CH3COOH+H2O?CH3COO-+H3O+ | |
| D�� | ����ˮ������Ӧ2Fe+3H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe2O3+3H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����8.0g | B�� | ����8.00g | C�� | ����8.0g | D�� | ����0.2g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com