
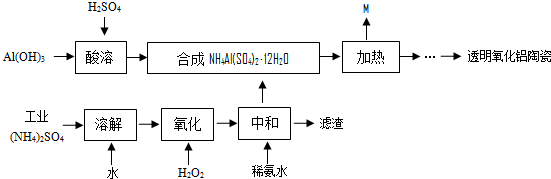
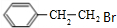 £»EµÄ·Ö×ÓŹ½ĪŖC10H12O2£»FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢õ„»ł£®
£»EµÄ·Ö×ÓŹ½ĪŖC10H12O2£»FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢õ„»ł£® £®
£® Öʱø
Öʱø 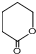 µÄŗĻ³ÉĀ·ĻßĮ÷³Ģ
µÄŗĻ³ÉĀ·ĻßĮ÷³Ģ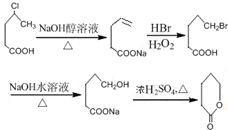 £®
£® ·ÖĪö øł¾ŻŗĻ³ÉĻßĀ·æÉÖŖ£¬DÓėŠĀÖĘCu£ØOH £©2¼ÓČČĢõ¼žĻĀ·“Ó¦£¬Ėį»ÆŗóµĆ±½ŅŅĖį£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £»C“ß»ÆŃõ»ÆÉś³ÉD£¬ŌņCµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£»C“ß»ÆŃõ»ÆÉś³ÉD£¬ŌņCµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £»BĖ®½āÉś³ÉC£¬ŌņBµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
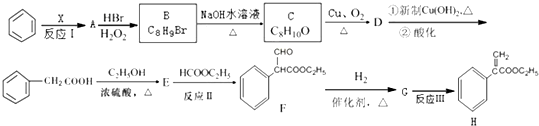
£»BĖ®½āÉś³ÉC£¬ŌņBµÄ½į¹¹¼ņŹ½ĪŖ£ŗ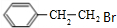 £»AÓėäå»ÆĒāŌŚĖ«ŃõĖ®µÄ×÷ÓĆĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬ĖłŅŌAĪŖ±½ŅŅĻ©£¬·“Ó¦¢ńĖłÉę¼°µÄĪļÖŹ¾łĪŖĢž£¬ĒāµÄÖŹĮæ·ÖŹż¾łĻąĶ¬£¬±Č½Ļ±½ÓėAµÄ½į¹¹æÉÖŖ£¬±½ÓėX·¢Éś¼Ó³É·“Ӧɜ³ÉA£¬ĖłŅŌXĪŖCH”ŌCH£¬±½ŅŅĖįÓėŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ
£»AÓėäå»ÆĒāŌŚĖ«ŃõĖ®µÄ×÷ÓĆĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬ĖłŅŌAĪŖ±½ŅŅĻ©£¬·“Ó¦¢ńĖłÉę¼°µÄĪļÖŹ¾łĪŖĢž£¬ĒāµÄÖŹĮæ·ÖŹż¾łĻąĶ¬£¬±Č½Ļ±½ÓėAµÄ½į¹¹æÉÖŖ£¬±½ÓėX·¢Éś¼Ó³É·“Ӧɜ³ÉA£¬ĖłŅŌXĪŖCH”ŌCH£¬±½ŅŅĖįÓėŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ £¬E·¢ÉśČ”“ś·“Ӧɜ³ÉF£¬FÓėĒāĘų·¢Éś¼Ó³É£¬Č©»ł×Ŗ»ÆĪŖōĒ»ł£¬ŌņGµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬E·¢ÉśČ”“ś·“Ӧɜ³ÉF£¬FÓėĒāĘų·¢Éś¼Ó³É£¬Č©»ł×Ŗ»ÆĪŖōĒ»ł£¬ŌņGµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬G·¢ÉśĻūČ„·“Ӧɜ³ÉH£¬ÓÉ
£¬G·¢ÉśĻūČ„·“Ӧɜ³ÉH£¬ÓÉ Öʱø
Öʱø  £¬æÉŅŌÓĆ
£¬æÉŅŌÓĆ ŅĄ“ĪĶعżĻūČ„·“Ó¦µĆµ½Ģ¼Ģ¼Ė«¼ü£¬ŌŚH2O2Ģõ¼žĻĀÓėHBr¼Ó³É£¬BrŌŚ¶ĖµćµÄCŌ×ÓÉĻ£¬Ė®½ā·“Ӧɜ³É-OH£¬Č»ŗó·¢Éśõ„»Æ·“Ó¦µĆ×īÖÕ²śĪļ£¬¾Ż“Ė½ųŠŠ½ā“š£®
ŅĄ“ĪĶعżĻūČ„·“Ó¦µĆµ½Ģ¼Ģ¼Ė«¼ü£¬ŌŚH2O2Ģõ¼žĻĀÓėHBr¼Ó³É£¬BrŌŚ¶ĖµćµÄCŌ×ÓÉĻ£¬Ė®½ā·“Ӧɜ³É-OH£¬Č»ŗó·¢Éśõ„»Æ·“Ó¦µĆ×īÖÕ²śĪļ£¬¾Ż“Ė½ųŠŠ½ā“š£®
½ā“š ½ā£ŗøł¾ŻŗĻ³ÉĻßĀ·æÉÖŖ£¬DÓėŠĀÖĘCu£ØOH £©2¼ÓČČĢõ¼žĻĀ·“Ó¦£¬Ėį»ÆŗóµĆ±½ŅŅĖį£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £»C“ß»ÆŃõ»ÆÉś³ÉD£¬ŌņCµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£»C“ß»ÆŃõ»ÆÉś³ÉD£¬ŌņCµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £»BĖ®½āÉś³ÉC£¬ŌņBµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£»BĖ®½āÉś³ÉC£¬ŌņBµÄ½į¹¹¼ņŹ½ĪŖ£ŗ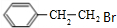 £»AÓėäå»ÆĒāŌŚĖ«ŃõĖ®µÄ×÷ÓĆĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬ĖłŅŌAĪŖ±½ŅŅĻ©£¬·“Ó¦¢ńĖłÉę¼°µÄĪļÖŹ¾łĪŖĢž£¬ĒāµÄÖŹĮæ·ÖŹż¾łĻąĶ¬£¬±Č½Ļ±½ÓėAµÄ½į¹¹æÉÖŖ£¬±½ÓėX·¢Éś¼Ó³É·“Ӧɜ³ÉA£¬ĖłŅŌXĪŖCH”ŌCH£¬±½ŅŅĖįÓėŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ
£»AÓėäå»ÆĒāŌŚĖ«ŃõĖ®µÄ×÷ÓĆĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬ĖłŅŌAĪŖ±½ŅŅĻ©£¬·“Ó¦¢ńĖłÉę¼°µÄĪļÖŹ¾łĪŖĢž£¬ĒāµÄÖŹĮæ·ÖŹż¾łĻąĶ¬£¬±Č½Ļ±½ÓėAµÄ½į¹¹æÉÖŖ£¬±½ÓėX·¢Éś¼Ó³É·“Ӧɜ³ÉA£¬ĖłŅŌXĪŖCH”ŌCH£¬±½ŅŅĖįÓėŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ £¬E·¢ÉśČ”“ś·“Ӧɜ³ÉF£¬FÓėĒāĘų·¢Éś¼Ó³É£¬Č©»ł×Ŗ»ÆĪŖōĒ»ł£¬ŌņGµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬E·¢ÉśČ”“ś·“Ӧɜ³ÉF£¬FÓėĒāĘų·¢Éś¼Ó³É£¬Č©»ł×Ŗ»ÆĪŖōĒ»ł£¬ŌņGµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬G·¢ÉśĻūČ„·“Ӧɜ³ÉH£¬
£¬G·¢ÉśĻūČ„·“Ӧɜ³ÉH£¬
£Ø1£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬AĪŖ±½ŅŅĻ©£¬±½ŅŅĻ©·Ö×ÓÖŠ“¦ÓŚ¶ŌĪ»µÄ×ī¶ąÓŠ3øöĢ¼Ō×ÓŌŚŅ»ĢõÖ±ĻßÉĻ£¬¹Ź“š°øĪŖ£ŗ±½ŅŅĻ©£»3£»
£Ø2£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬·“Ó¦¢ņµÄ·“Ó¦ĄąŠĶŹĒ Č”“ś·“Ó¦£¬·“Ó¦¢óµÄ·“Ó¦ĄąŠĶŹĒĻūČ„·“Ó¦£¬¹Ź“š°øĪŖ£ŗČ”“ś·“Ó¦£»ĻūČ„·“Ó¦£»
£Ø3£©BµÄ½į¹¹¼ņŹ½ĪŖ£ŗ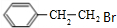 £¬EĪŖ
£¬EĪŖ £¬EµÄ·Ö×ÓŹ½ĪŖ C10H12O2£¬øł¾ŻFµÄ½į¹¹¼ņŹ½æÉÖŖ£¬FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢õ„»ł£¬
£¬EµÄ·Ö×ÓŹ½ĪŖ C10H12O2£¬øł¾ŻFµÄ½į¹¹¼ņŹ½æÉÖŖ£¬FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢õ„»ł£¬
¹Ź“š°øĪŖ£ŗ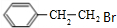 £»C10H12O2£»Č©»ł”¢õ„»ł£»
£»C10H12O2£»Č©»ł”¢õ„»ł£»
£Ø4£©ÓÉC”śD·“Ó¦ŹĒ “ß»ÆŃõ»Æ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
“ß»ÆŃõ»Æ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø5£©GµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬»ÆŗĻĪļGĖįŠŌĢõ¼žĻĀĖ®½ā²śĪļÖ®Ņ»MĪŖ
£¬»ÆŗĻĪļGĖįŠŌĢõ¼žĻĀĖ®½ā²śĪļÖ®Ņ»MĪŖ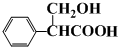 £¬
£¬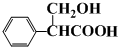 ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼ž£ŗÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ŗ¬ÓŠ·ÓōĒ»ł£»ÄÜ·¢ÉśĖ®½ā·“Ó¦ŗĶŅų¾µ·“Ó¦£¬ŗ¬ÓŠ¼×ĖįŠĪ³ÉµÄõ„»ł£¬±½»·ÉĻÓŠČżøöČ”“ś»ł£¬·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåĪŖ±½»·ÉĻĮ¬ÓŠ-OH”¢HCOO-”¢CH3CH2-£¬»ņ-OH”¢HCOOCH2-”¢CH3-£¬øł¾Ż¶Ø¶ž¶ÆŅ»µÄŌŌņ£¬ĆæÖÖ¶¼ÓŠ10ÖÖ½į¹¹£¬ĖłŅŌ¹²ÓŠ20ÖÖ½į¹¹£¬
ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼ž£ŗÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ŗ¬ÓŠ·ÓōĒ»ł£»ÄÜ·¢ÉśĖ®½ā·“Ó¦ŗĶŅų¾µ·“Ó¦£¬ŗ¬ÓŠ¼×ĖįŠĪ³ÉµÄõ„»ł£¬±½»·ÉĻÓŠČżøöČ”“ś»ł£¬·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåĪŖ±½»·ÉĻĮ¬ÓŠ-OH”¢HCOO-”¢CH3CH2-£¬»ņ-OH”¢HCOOCH2-”¢CH3-£¬øł¾Ż¶Ø¶ž¶ÆŅ»µÄŌŌņ£¬ĆæÖÖ¶¼ÓŠ10ÖÖ½į¹¹£¬ĖłŅŌ¹²ÓŠ20ÖÖ½į¹¹£¬
¹Ź“š°øĪŖ£ŗ20£»
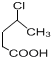
£Ø5£©ÓÉ Öʱø
Öʱø  £¬æÉŅŌÓĆ
£¬æÉŅŌÓĆ ŅĄ“ĪĶعżĻūČ„·“Ó¦µĆµ½Ģ¼Ģ¼Ė«¼ü£¬ŌŚH2O2Ģõ¼žĻĀÓėHBr¼Ó³É£¬BrŌŚ¶ĖµćµÄCŌ×ÓÉĻ£¬Ė®½ā·“Ӧɜ³É-OH£¬Č»ŗó·¢Éśõ„»Æ·“Ó¦µĆ×īÖÕ²śĪļ£¬ĖłŅŌŗĻ³ÉĀ·ĻßĶ¼ĪŖ£ŗ
ŅĄ“ĪĶعżĻūČ„·“Ó¦µĆµ½Ģ¼Ģ¼Ė«¼ü£¬ŌŚH2O2Ģõ¼žĻĀÓėHBr¼Ó³É£¬BrŌŚ¶ĖµćµÄCŌ×ÓÉĻ£¬Ė®½ā·“Ӧɜ³É-OH£¬Č»ŗó·¢Éśõ„»Æ·“Ó¦µĆ×īÖÕ²śĪļ£¬ĖłŅŌŗĻ³ÉĀ·ĻßĶ¼ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śŗĻ³É£¬ĢāÄæÄѶČÖŠµČ£¬ŹŌĢāÉę¼°ÓŠ»ś·“Ó¦ĄąŠĶ”¢Ķ¬·ÖŅģ¹¹ĢåŹéŠ“”¢ÓŠ»ś·“Ó¦·½³ĢŹ½µČÖŖŹ¶£¬×¢Ņāøł¾Ż·“Ó¦Ģõ¼ž½ųŠŠĶʶĻ£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕ¹ŁÄÜĶŵĊŌÖŹÓė×Ŗ»Æ£¬£Ø5£©ÖŠĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“ĪŖŅדķµć”¢ÄŃµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
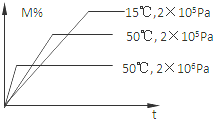 ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ·“Ó¦£ŗM£Øg£©+N£Øg£©?R£Øg£©+2L£¬“Ė·“Ó¦·ūŗĻĻĀĶ¼¹ŲĻµ£¬øĆ·“Ó¦ŹĒĻĀĮŠÄÄÖÖĒéæö£Ø””””£©
ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ·“Ó¦£ŗM£Øg£©+N£Øg£©?R£Øg£©+2L£¬“Ė·“Ó¦·ūŗĻĻĀĶ¼¹ŲĻµ£¬øĆ·“Ó¦ŹĒĻĀĮŠÄÄÖÖĒéæö£Ø””””£©| A£® | Õż·“Ó¦ĪüČČ£¬LŹĒ¹ĢĢå»ņŅŗĢå | B£® | Õż·“Ó¦ĪüČČ£¬LŹĒĘųĢå | ||
| C£® | Õż·“Ó¦·ÅČČ£¬LŹĒ¹ĢĢå»ņŅŗĢå | D£® | Õż·“Ó¦·ÅČČ£¬LŹĒĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
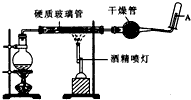 ŌŚ³£ĪĀĻĀ£¬FeÓėĖ®²¢²»Ęš·“Ó¦£¬µ«ŌŚøßĪĀĻĀ£¬FeÓėĖ®ÕōĘųæÉ·¢Éś·“Ó¦£® Ó¦ÓĆĻĀĮŠ×°ÖĆ£¬ŌŚÓ²ÖŹ²£Į§¹ÜÖŠ·ÅČė»¹ŌĢś·ŪŗĶŹÆĆŽČŽµÄ»ģŗĻĪļ£¬¼ÓČČ£¬²¢ĶØČėĖ®ÕōĘų£¬¾ĶæÉŅŌĶź³ÉøßĪĀĻĀ”°FeÓėĖ®ÕōĘųµÄ·“Ó¦ŹµŃé”±£® Ēė»Ų“šøĆŹµŃéÖŠµÄĪŹĢā£®
ŌŚ³£ĪĀĻĀ£¬FeÓėĖ®²¢²»Ęš·“Ó¦£¬µ«ŌŚøßĪĀĻĀ£¬FeÓėĖ®ÕōĘųæÉ·¢Éś·“Ó¦£® Ó¦ÓĆĻĀĮŠ×°ÖĆ£¬ŌŚÓ²ÖŹ²£Į§¹ÜÖŠ·ÅČė»¹ŌĢś·ŪŗĶŹÆĆŽČŽµÄ»ģŗĻĪļ£¬¼ÓČČ£¬²¢ĶØČėĖ®ÕōĘų£¬¾ĶæÉŅŌĶź³ÉøßĪĀĻĀ”°FeÓėĖ®ÕōĘųµÄ·“Ó¦ŹµŃé”±£® Ēė»Ų“šøĆŹµŃéÖŠµÄĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ėį | µēĄėĘ½ŗā³£ŹżK |
| CH3COOH | 1.76”Į10-5 |
| H2CO3 | K1=4.3”Į10-7 K2=5.61”Į10-11 |
| H3PO4 | K1=7.52”Į10-3 K2=6.23”Į10-8 K3=2.20”Į10-13 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼ĪŖĻą»„“®ĮŖµÄ¼×ŅŅĮ½øöµē½ā³Ų£¬Ēė»Ų“š£ŗ
ČēĶ¼ĪŖĻą»„“®ĮŖµÄ¼×ŅŅĮ½øöµē½ā³Ų£¬Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé²½Öč£Ø²»ŅŖĒ󊓳ö¾ßĢå²Ł×÷¹ż³Ģ£© | Ō¤ĘŚŹµŃéĻÖĻóŗĶ½įĀŪ |
| ȔɣĮæŗŚÉ«¹ĢĢ壬¼ÓČėŹŹĮæĻ”ŃĪĖį»ņĻ”ĮņĖį£¬ ŌŚČÜŅŗÖŠ¼ÓČėĮņĒč»Æ¼ŲČÜŅŗ | ČÜŅŗ²»±äŗģÉ«£¬Ōņ¼ŁÉčŅ»³ÉĮ¢£¬ ČÜŅŗ±ä³ÉŗģÉ«£¬Ōņ¼ŁÉčŅ»²»³ÉĮ¢ |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2ŹōÓŚ¼īŠŌŃõ»ÆĪļ | |
| B£® | ĖįÓźŹĒpHŠ”ÓŚ7µÄÓźĖ® | |
| C£® | CO2”¢NO2»ņSO2¶¼»įµ¼ÖĀĖįÓźµÄŠĪ³É | |
| D£® | “óĪķŹĒŅ»ÖÖ½ŗĢ壬ÄÜ·¢Éś¶”“ļ¶ūŠ§Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com