
| A. | 浓硝酸中滴入碳酸钠溶液中 | B. | 铜与浓硝酸反应 | ||
| C. | 氢氧化亚铁与浓硝酸反应 | D. | 碳与浓硝酸反应 |
分析 硝酸既表现酸性,又表现氧化性,说明反应过程中部分硝酸中元素化合价不变,部分硝酸中得电子化合价降低,根据元素化合价来分析解答.
解答 解:A.浓硝酸中滴入碳酸钠溶液中发生复分解反应,只表现硝酸的酸性,故A正确;
B.Cu+HNO3中N元素部分化合价降低,部分不变,化合价降低时表现氧化性,生成硝酸铜时表现酸性,故B错误;
C.氧化亚铁和浓硝酸反应生成硝酸铁、二氧化氮和水,其中生成三价铁盐表现硝酸氧化性和酸性,故C错误;
D.C和HNO3反应生成二氧化碳、二氧化氮和水,发生C+4HNO3=CO2↑+2H2O+4NO2↑,硝酸只表现出强氧化性,故D错误;
故选A.
点评 本题考查硝酸的性质,注意分析反应中N元素的化合价是否变化,明确硝酸的氧化性是由N元素的化合价降低体现的,生成硝酸盐体现酸性是解答本题的关键,题目难度不大.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 往盛有500mL1mol/L的Na2CO3的溶液中滴加稀盐酸,可以观察到立即产生大量气泡 | |
| B. | 100mL 0.5mol/L氯酸钾溶液中含有氯离子的物质的量是0.05mol | |
| C. | 在开放的环境中往含有Fe2+,Al3+,Mg2+,Na+的溶液中滴加NaOH溶液,最终可以得到4种沉淀 | |
| D. | H+,NO3-,Fe2+,Mg2+不能共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| B. | 铁溶于盐酸中:Fe+6H+═Fe3++3H2↑ | |
| C. | 氯化铝溶液和氨水反应 Al3++NH3•H2O═Al(OH)3↓+NH4+ | |
| D. | NaHCO3溶液与HCl溶液反应:H++HCO3-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
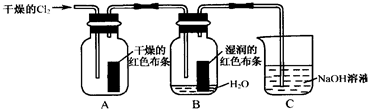
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量HSO3-的澄清透明溶液中:K+、OH-、Cl-、Na+ | |
| B. | 能使无色酚酞变红的溶液中:Ca2+、NH4+、Cl-、Fe2+ | |
| C. | 有NO3-存在的强酸性溶液中:Na+、Mg2+、I-、Br- | |
| D. | 能与Fe反应放出大量H2的溶液:Al3+、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
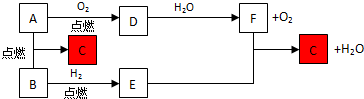
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com