
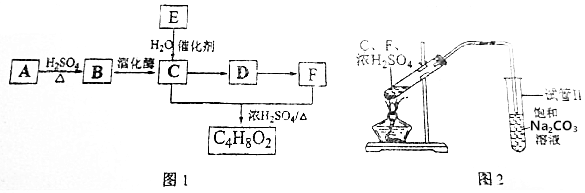
分析 A、B、C是食品中常见的有机物,均只含C、H、O三种元素,其中A是天然高分子化合物,B、D均能与含氢氧化钠的氢氧化铜悬浊液反应,可知A为(C6H10O5)n,A水解生成B为葡萄糖(C6H12O6),C为CH3CH2OH,E为CH2=CH2,D为CH3CHO,F为CH3COOH,C与F发生酯化反应生成CH3COOCH2CH3,以此来解答.
解答 解:(1)A.分馏得到饱和烃,故A不选;
B.干馏与煤有关,故B不选;
C.石油裂解可得到乙烯,故C选;
D.石油裂化得到汽油,故D不选;
故答案为:C;
(2)F中所含官能团的名称是羧基,E→C的反应类型为CH2=CH2的加成反应,
故答案为:羧基;加成反应;
(3)C→D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(4)A.饱和碳酸钠溶液可以除去产物中混有的乙醇和乙酸,与乙酸乙酯分层,操作合理,故A正确;
B.浓硫酸可吸收水,该反应为可逆反应,则浓硫酸的作用是催化剂和吸水剂,故B正确;
C.产物为乙酸乙酯,是一种无色透明不溶于水,密度比水小的液体,与水混合在上层,故C错误;
故答案为:C.
点评 本题考查有机物的合成,为高频考点,把握B为葡萄糖、D为乙醛为解答的关键,侧重分析与推断能力的考查,注意有机物性质的应用,题目难度中等.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 不慎碰倒酒精灯,洒出酒精在桌上燃烧,应立即用湿抹布扑盖 | |
| B. | 将一氧化碳中毒者移到通风处抢救 | |
| C. | 实验后,剩余的药品不能放回原瓶,也不能随便丢弃 | |
| D. | 不慎把浓碱溅在皮肤上,用大量水冲洗后,再涂上碳酸氢钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 1.00 | 0.70 | 0.50 | 0.20 | 0.20 |
| T2 | n(CH4)/mol | 1.00 | 0.60 | 0.36 | … | 0.30 |
| A. | T2时NO2的平衡转化率为70.0% | |
| B. | 该反应的△H<0、T1<T2 | |
| C. | 保持其他条件不变,T1时向平衡体系中再充入1.00molCH4和2.40molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小 | |
| D. | 保持其他条件不变,T1时向平衡体系中再充入0.60molCH4和1.60molH2O(g),平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子只能在电子云轮廓图中运动 | |
| B. | 能层不同,电子云轮廓图形状不相同 | |
| C. | 轨道数目相同,电子云轮廓图形状、大小完全相同 | |
| D. | 能层不同,能级相同,电子云轮廓图形状相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
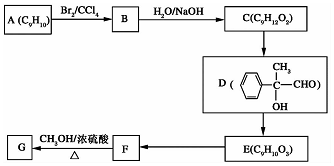
 .
.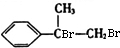 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$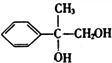 +2NaBr
+2NaBr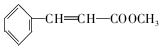 互为同分异构体
互为同分异构体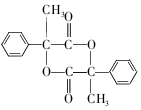 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.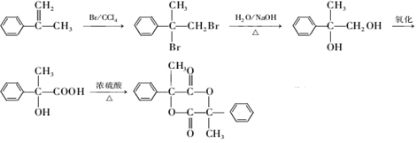 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
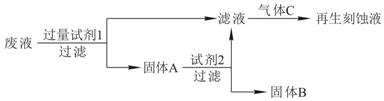
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 单质 | 氧化物 | 酸 | 碱 | 盐 | |
| A | 钠 | 水 | 硝酸 | 小苏打 | 胆矾 |
| B | 生铁 | 硅酸钠 | H2SiO3 | KOH | NH4Cl |
| C | 晶体硅 | 过氧化钠 | 盐酸 | '纯碱 | 明矾 |
| D | 液氯 | 铁红 | 硫酸 | Ca(OH)2 | Na2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广和鼓励多使用公共交通工具出行 | |
| B. | 植树造林,绿化环境 | |
| C. | 利用廉价煤炭,大力发展火力发电 | |
| D. | 对燃煤进行脱硫,减少空气的污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com