
| 类别组合 | 酸性氧化物 | 碱性氧化物 | 电解质 | 强电解质 | 高分子物质 |
| A | CO2 | CuO | 氨气 | NH3?H2O | 葡萄糖 |
| B | SO3 | Na2O | 稀硫酸 | NaOH | 果糖 |
| C | SO2 | CaO | 冰醋酸 | KOH | 纤维素 |
| D | N2O5 | Na2O2 | α-丙氨酸 | Cu(OH)2 | 聚乙烯 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、1 mol?L-1的甲酸溶液的c(H+)为1×10-2 mol?L-1 |
| B、甲酸能与水以任意比互溶 |
| C、10 mL 1 mol?L-1的甲酸溶液恰好与10 mL 1 mol?L-1的NaOH溶液完全反应 |
| D、滴入石蕊溶液显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在Na2CO3溶液中通入少量CO2 :CO32-+CO2+H2O═2HCO3- | ||||
B、用惰性电极电解 MgCl2 溶液:2Cl-+2H2O
| ||||
| C、在NaHSO4溶液中滴加Ba(OH)2 溶液至中性:H++SO42-+Ba2++OH-═BaSO4 ↓+H2O | ||||
| D、CaSO3 溶于稀硝酸中:CaSO3 +2H+═Ca2++SO2 ↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、N原子的最外层电子轨道表示式: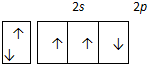 | ||
B、质子数为35、中子数为45的溴原子:
| ||
C、硫离子的结构示意图: | ||
D、间二甲苯的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾 | |
| 体积 (mL) | 浓度 (mol?L-1) | |||
| 1 | 25 | 0.5 | 4.00 | 0.1000 |
| 2 | 50 | 0.5 | 4.00 | 0.1000 |
| 3 | 25 | 0.5 | 4.00 | 0.0100 |
| 4 | 25 | 0 | 4.00 | 0.1000 |
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+NH4+Cl-NO3- |
| B、Cu2+H+HCO3-Cl- |
| C、Fe3+H+Cl-SCN- |
| D、Ba2+H+NO3-Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 且a、b、c、d均大于零,则下列说法正确的是( )
且a、b、c、d均大于零,则下列说法正确的是( )| A、断开1molH-Cl键所需的能量为-a-b-c |
| B、b>c,则氢气分子具有的能量高于氯气分子具有的能量 |
| C、Cl2(s)=Cl2(g)△H=+(a+d)kJ?mol-1 |
| D、向1molCl2(g)中通入1molH2(g),发生反应时放热dkJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com