
| A. | 50mL 1.5mol•L-1的CaCl2溶液 | B. | 100mL 3mol•L-1的NH4Cl溶液 | ||
| C. | 75mL 3mol•L-1的KCl溶液 | D. | 50mL 2mol•L-1的FeCl2溶液 |
分析 50mL 1mol•L-1的FeCl3溶液中氯离子物质的量为0.05L×1mol/L×3=0.15mol,溶液中离子的物质的量相等,则离子数目一定相等,根据n=c•V结合化合物的组成计算;根据化学式可知1mol•L-1的FeCl3溶液中氯离子浓度为3mol/L,结合各选项中化学式判断溶液中氯离子浓度,注意离子的浓度与溶液的体积无关,与物质的构成有关.
解答 解:50mL 1mol•L-1的FeCl3溶液中氯离子物质的量为0.05L×1mol/L×3=0.15mol,氯离子浓度是3mol/L.
A、50mL 1.5mol•L-1的CaCl2溶液中氯离子物质的量为0.05L×1.5mol/L×2=0.15mol,氯离子浓度是3mol/L,故A正确;
B、100mL 3mol•L-1的NH4Cl溶液中氯离子物质的量为0.1L×3mol/L=0.3mol,氯离子浓度是3mol/L,故B错误;
C、75mL3mol•L-1的KCl溶液中氯离子物质的量为0.075L×3mol/L=0.225mol,氯离子浓度是3mol/L,故C错误;
D、50mL2mol•L-1的FeCl2溶液中氯离子物质的量为0.05L×2mol/L×2=0.2mol,氯离子浓度是4mol/L,故D错误.
故选A.
点评 本题考查物质的量浓度的计算,明确物质的构成是解答本题的关键,题目难度不大,注意物质的量与质量、浓度等物理量的计算公式的运算、离子的浓度与溶液的体积无关,与物质的构成有关.


科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 分子式为C3H7Br的有机物甲在适宜的条件下能发生如下一系列转化:
分子式为C3H7Br的有机物甲在适宜的条件下能发生如下一系列转化: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol/L醋酸 | B. | 0.1 L 0.1 mol/L H3PO4溶液 | ||
| C. | 0.5 L 0.1 mol/L盐酸 | D. | 2 L 0.1 mol/L H2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  反应Ⅰ:△H>0,P2>P1 | B. |  反应Ⅱ:△H<0,T1<T2 | ||
| C. | 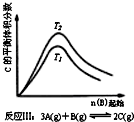 反应Ⅲ:△H<0,T2>T1;或△H>0,T2<T1 | D. | 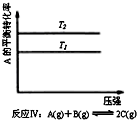 反应Ⅳ:△H<0,T2<T1或△H>0,T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图①用于实验室制乙烯 | |
| B. | 图②用于实验室制乙炔并验证乙炔可以发生氧化反应 | |
| C. | 图③用于实验室中分馏石油 | |
| D. | 图④中若A为醋酸,B为贝壳,C为苯酚钠溶液,则可验证醋酸的酸性大于碳酸,但不能验证碳酸的酸性大于苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1L乙醇完全燃烧产生CO2分子的数目为$\frac{{N}_{A}}{22.4}$×2 | |
| B. | 磷酸的摩尔质量与NA个磷酸分子的质量之和相等 | |
| C. | 16gO2、O3的混合物所含的氧原子数目为NA | |
| D. | 1molOH-所含的质子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4、Na2O、MgCl2、CO2 | B. | NaHCO3、Ba(OH)2、Na2CO3、ZnO | ||
| C. | HNO3、Ca(OH)2、Na2CO3、SO3 | D. | HCl、KOH、Na2CO3、MgO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com