
实验室制备溴乙烷(C2H5Br)的原理为C2H5OH+NaBr+H2SO4![]() NaHSO4+C2H5Br+H2O,装置如图(已知溴乙烷的沸点38.4℃)和步骤如下:
NaHSO4+C2H5Br+H2O,装置如图(已知溴乙烷的沸点38.4℃)和步骤如下:
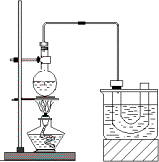
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;②在圆底烧瓶中加入研细的13 g溴化钠和几粒碎瓷片,然后加入10 mL 95%乙醇、28 mL 78%浓硫酸;③小心加热,使其充分反应.
回答下列问题:
(1)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为________
(2)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是________.
(3)U型管内可观察到的现象是________.
(4)反应结束后,U形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的________(填序号).
A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
所需的主要玻璃仪器是________(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗、分液,然后向油层中加入无水CaCl2,再进行________(填操作名称).
(5)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后________(填代号).
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:阅读理解
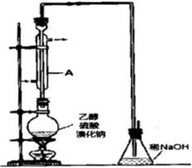 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是查看答案和解析>>
科目:高中化学 来源: 题型:
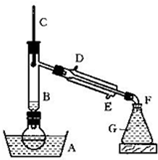 蒸出的溴乙烷用水下收集法获得.可能发生的副反应:H2SO4(浓)+2HBr→Br2+SO2+2H2O
蒸出的溴乙烷用水下收集法获得.可能发生的副反应:H2SO4(浓)+2HBr→Br2+SO2+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:
 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应实际通常是用溴化钠与一定浓度的硫酸和乙醇反应.某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步 骤如下:
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应实际通常是用溴化钠与一定浓度的硫酸和乙醇反应.某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步 骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g?cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
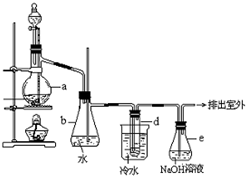 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4°C,密度为1.43g?ml-1;
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4°C,密度为1.43g?ml-1;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com