
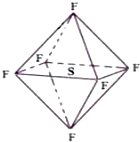
 六氟化硫分子呈正八面体形(如图所示),在高电压下仍有良好的绝缘性,在电器工业方面有着广泛的用途,但逸散到空气中会引起温室效应,下列有关六氟化硫的推测正确的是( )
六氟化硫分子呈正八面体形(如图所示),在高电压下仍有良好的绝缘性,在电器工业方面有着广泛的用途,但逸散到空气中会引起温室效应,下列有关六氟化硫的推测正确的是( )| A. | 六氟化硫易燃烧生成二氧化硫 | |
| B. | 六氟化硫中各原子均达到8电子稳定结构 | |
| C. | 六氟化硫分子中的S-F键都是σ键,且键长、键能都相等 | |
| D. | 六氟化硫分子是极性分子 |
分析 A.SF6中F为-1价,则S为+6价,S元素不能再失电子,所以不能被氧化;
B.根据图片知,每个F原子和S原子形成一对共用电子对,每个S原子和六个F原子形成六对共用电子对;
C.六氟化硫分子中的S-F键都是σ键,为正八面体结构,键长、键能都相等;
D.结构对称且正负电荷中心重合的分子为非极性分子.
解答 解:A.SF6中F为-1价,则S为+6价,S元素不能再失电子,所以不能被氧化,则六氟化硫不易燃烧生成二氧化硫,故A错误;
B.根据图片知,每个F原子和S原子形成一对共用电子对,每个S原子和六个F原子形成六对共用电子对,所以F原子都达到8电子稳定结构,但S原子最外层达到12电子,故B错误;
C.六氟化硫分子中的S-F键都是σ键,为正八面体结构,所以键长、键能都相等,故C正确;
D.该分子为正八面体结构,正负电荷中心重合,为非极性分子,故D错误;
故选C.
点评 本题考查分子极性判断、8电子稳定结构判断、物质性质等知识点,为高考高频点,侧重考查学生观察、获取信息、运用信息能力,易错选项是A,很多同学往往认为含有硫元素就能燃烧而导致错误判断.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
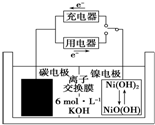 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为H2-2e-═2H+ | |
| D. | 放电时镍电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{3a}{2B}$mol/L | B. | $\frac{a}{27B}$mol/L | C. | $\frac{a}{18B}$mol/L | D. | $\frac{2a}{81B}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 7:2 | B. | 4:5 | C. | 5:4 | D. | 2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
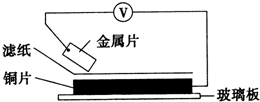 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( )
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( ) | 金属 | 电子流动方向 | 电压(V) |
| 甲 | 甲→Cu | +0.78 |
| 乙 | Cu→乙 | -0.15 |
| 丙 | 丙→Cu | +1.35 |
| 丁 | E→Cu | +0.30 |
| A. | 金属乙能从硫酸铜溶液中置换出铜 | |
| B. | 甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀 | |
| C. | 在四种金属中乙的还原性最强 | |
| D. | 甲、丁若形成原电池时,甲为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
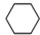 (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$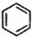 (g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )
(g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )| A. |  | B. | 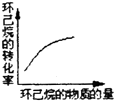 | C. | 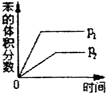 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
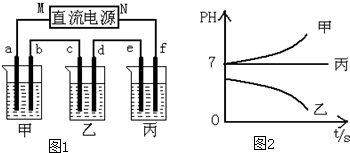
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||
 ,③与①所形成的化合物的结构式为:
,③与①所形成的化合物的结构式为: .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com