
 一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:mA(s)+nB(g)?pC(g)+q(D)g.达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L.当其条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是( )
一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:mA(s)+nB(g)?pC(g)+q(D)g.达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L.当其条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是( )| A、容积扩大到原来的两倍,平衡向逆反应方向移动 |
| B、化学方程式中n>p+q |
| C、达到平衡后,若升高温度,平衡向逆反应方向移动 |
| D、达到平衡后,增加A的量,有利于提高B的转化率 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 操作 | 现象 |
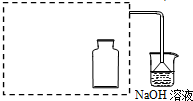
| a.用干燥洁净的烧杯取约10mL浓硝酸,加热. |  |
| b.把小块烧红的木炭迅速伸入热的浓硝酸中. | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.4mol/L |
| B、0.2mol/L |
| C、1.8mol/L |
| D、3.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
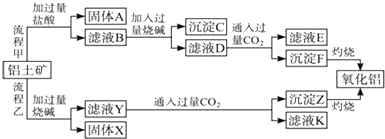
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn为负极,MnO2为正极 |
| B、Zn为正极,MnO2为负极 |
| C、工作时电子由MnO2经外电路流向Zn极 |
| D、Zn电极发生还原反应,MnO2电极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、45kJ |
| B、436kJ |
| C、1308kJ |
| D、135kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com