
| 反应 | A | B | C | D |
| △H/kJ?mol-1 | 10.5 | 1.80 | -126 | -11.7 |
| △S/J?mol-1?K-1 | 30.0 | -113.0 | 84.0 | -105.0 |


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
| A、选择毒性、刺激性较小的染发剂,如植物性染发剂,减少染发剂对人体的伤害 |
| B、染发时应严格遵守染发剂使用说明,不要混合使用不同的染发剂 |
| C、尽量少染发,当头皮有伤口时不要染发 |
| D、染完头发后,不必清洗多次,以免影响染发效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
12 6 |
13 6 |

查看答案和解析>>
科目:高中化学 来源: 题型:
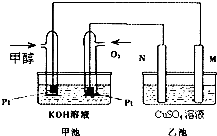 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出直接以甲醇为燃料的燃料电池.如图中甲池是一个甲醇燃料电池工作时的示意图.乙池中的两个电极均为石墨电极,乙池中盛有100mL 3.00mol.L-1的CuSO4溶液.已知H2(g)、CO(g)和CH3OH(l)的热值分别为143kJ?g-1、10kJ?g-1和23kJ?g-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出直接以甲醇为燃料的燃料电池.如图中甲池是一个甲醇燃料电池工作时的示意图.乙池中的两个电极均为石墨电极,乙池中盛有100mL 3.00mol.L-1的CuSO4溶液.已知H2(g)、CO(g)和CH3OH(l)的热值分别为143kJ?g-1、10kJ?g-1和23kJ?g-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
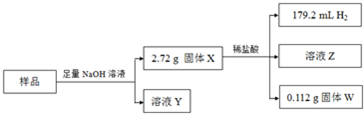
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加入AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加入足量NaOH溶液并加热 | 收集到气体1.12L(换算成标准状况) |
| 3 | 加入足量BaCl2溶液,将所得沉淀洗涤、干燥、称重;再向沉淀中加足量的稀盐酸,洗涤、干燥、称重 | 第一次称重读数为6.27g,第二次称重读数为2.33g |
查看答案和解析>>
科目:高中化学 来源: 题型:
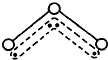 O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 3 |
| O | - 3 |
| O | - 3 |
| O | - 3 |
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加大太阳能、水能、风能、地热能等能源开发力度,减少化石燃料的使用 |
| B、研制乙醇汽油技术,降低机动车辆尾气中有害气体排放 |
| C、生产、生活中,努力实现资源的循环利用 |
| D、利用高新技术,提高石油、煤、天然气产量,以满足工业生产快速发展的需求 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com