
|
某酸溶液的pH=1,此酸溶液的物质的量浓度 | |
| [ ] | |
A. |
0.1 mol·L-1 |
B. |
一定大于0.1 mol·L-1 |
C. |
若为强酸一定等于0.1 mol·L-1,若为弱酸一定大于0.1 mol·L-1 |
D. |
若为强酸一定≤0.1 mol·L-1,若为弱酸一定>0.1 mol·L-1 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:013
某元素X的相对原子质量为a,它的最高价氧化物的水化物的化学式为HmXOn(m>1),下列有关叙述中正确的是
[ ]
A.该酸的水溶液中:c(H+)∶c(XOnm-)=m∶1
B.0.1mol·L-1该酸溶液的pH=1,则NamXOn的水溶液pH>7
C.该酸的摩尔质量为(m+a+16n)g
D.100ml该酸溶液只能中和4g NaOH
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高二化学 人教社(新课标B 2004年初审通过) 人教实验版 题型:013
|
某酸溶液的pH=3,则该酸溶液的物质的量浓度为 | |
| [ ] | |
A. |
一定大于0.001 mol·L-1 |
B. |
一定等于0.001 mol·L-1 |
C. |
一定小于0.001 mol·L-1 |
D. |
以上说法均欠妥 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
常温下,在某200 mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体, Fe的相对原子质量为56)。下列有关分析错误的是
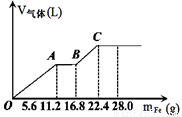
A、原混合酸中NO3-的物质的量为0.2 mol
B、原混合酸中H2SO4物质的量浓度为2mol/L
C、OA段与BC段反应中电子转移的物质的量之比为2:1
D、取20mL原混合酸加水稀释至1L后溶液的pH=1
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省内江市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
某研究小组探究:
I .铜片和浓硫酸的反应(夹持装置和A中加热装置已略,气密性已检验)
II. SO2 和 Fe( NO3)3 溶液的反应[1.0 mol/L 的 Fe(NO3)3 溶液的 pH=1] 请回答下列有关问题:
探究I
(l)某学进行了下列实验:取12.8g铜片和20 mL 18 mol•L-1的浓硫酸放在三颈瓶中共热,直至反应 完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。

①装置A中反应的化学方程式是_______
②该同学设计求余酸浓度的实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是______ (填字母)。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称貴
B.将产生的气体缓缓通入酸性髙锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定其产生气体的体积(折算成标准状况)
D.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
探究II
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是______。
(3)裝置B中产生了白色沉淀,分析B中产生白色沉淀的原因,提出下列三种猜想:
猜想1:SO2与Fe3+反应;猜想2 :在酸性条件下SO2与NO3-反应;猜想3:____________;
①按猜想1,装置B中反应的离子方程式是______,证明该猜想应进一步确认生成的新物质,其实验操作及现象是____________。
②按猜想2,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列某种溶液,在相同条件下进行实验。应选择的替换溶液是______ (填序号)。
a.0.1 mol/L 稀硝酸 b. 1.5 mol/L Fe(NO3)2 溶液
c. 6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com