
| A. | 锂离子电池充电时电池反应为C6Li+Li1-xMO2═LiMO2+C6Li1-x | |
| B. | 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量大 | |
| C. | 锂离子电池放电时电池内部Li+向负极移动 | |
| D. | 锂离子电池充电时阴极反应为C6Li1-x+xLi++xe-═C6Li |
分析 A.充电时电池反应式为放电电池反应式相反;
B.根据m=nM计算其质量;
C.放电时,电池内部阳离子向正极移动,阴离子向负极移动;
D.充电时,阴极上得电子发生还原反应,与放电时负极电极反应式相反.
解答 解:A.充电时电池反应式为放电电池反应式相反,放电时电池反应式为C6Li+Li1-xMO2=C6Li1-x+LiMO2,则充电时电池反应式为C6Li1-x+LiMO2=C6Li+Li1-xMO2,故A错误;
B.电池反应中,锂、锌、银、铅各失去1 mol 电子,消耗这几种金属的物质的量分别是1mol、0.5mol、1mol、0.5mol,根据m=nM知,消耗其质量分别是7g、32.5g、108g、103.5g,所以消耗Li质量最小,故B错误;
C.放电时,电池内部阳离子向正极移动,阴离子向负极移动,所以Li+向正极移动,故C错误;
D.充电时,阴极上得电子发生还原反应,与放电时负极电极反应式相反,则电极反应式为C6Li1-x+xLi++xe-═C6Li,故D正确.
故选D.
点评 本题考查原电池和电解池原理,明确蓄电池中正负极与阳极、阴极电极反应式关系是解本题关键,结合电池内部阴阳离子移动方向即可解答,题目难度中等.


科目:高中化学 来源: 题型:解答题
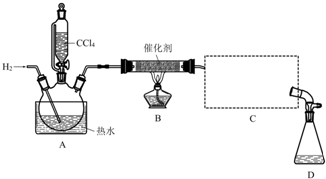
| 物质 | 相对分子质量 | 密度/(g•mL-1) | 沸点/℃ | 水中溶解性 |
| CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
| CCl4 | 154 | 1.59 | 76.7 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32g O2和O3的混合气体所含原子数为2NA | |
| B. | 100 mL 1 mol•L-1K2SO4溶液中含有的钾离子数为0.1NA | |
| C. | 10克氖气所含原子数约为6.02×1023 | |
| D. | 常温常压下,NA个H2分子的体积小于22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(正、H2)=υ(逆、HI) | |
| B. | 容器内的总压强不随时间而变化 | |
| C. | 单位时间内生成2n mol HI的同时,生成n mol的I2 | |
| D. | H2、I2、HI的反应速率比为2:2:1的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C不具有还原性 | |
| B. | 上述过程中砷元素发生还原反应 | |
| C. | 上述过程中+5价砷类物质作还原剂 | |
| D. | 1 mol+5价砷完全转化为+3价砷,共失去2 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | ② | ③ |
| ④ | ⑤ | ⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图1所示装置除去CO2中含有的少量HCl | |
| B. | 用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 | |
| C. | 用图3所示装置制取少量纯净的CO2气体 | |
| D. | 用图4所示装置高温煅烧石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、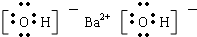 .
.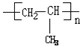 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com