
已知:Ka 为平衡常数,pKa=﹣lgKa,25℃时,H2A的 pKa1 =1.85,pKa2=7.19。用 0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如下图所示(曲线上的数字为 pH)。下列说法不正确的是
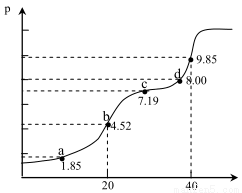
A.a 点所得溶液中;2c(H2A)+c(A2-)=0.002mol
B.b 点所得溶液中:c(H2 A)+c(H+)=c(A2-)+C(OH-)
C.C 点所得溶液中:c(Na+)<3c(HA-)
D.d 点所得溶液中:c(Na+)>c(A2-)>c(HA-)
科目:高中化学 来源:2015-2016学年吉林省松原市高一下期中化学试卷(解析版) 题型:选择题
将1molN2和3molH2进行合成氨试验后,测得反应后混合气体(N2、H2和NH3)的平均摩尔质量为10.2g·mol-1,则N2的转化率约为
A.18% B.20% C.25% D.33%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二5月调研二化学试卷(解析版) 题型:选择题
在一密闭容器中有CH4和O2混合气体共20g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重8g,则原混合气体中O2的质量分数是
A. 80% B.60% C.40% D.33.3%
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前押题理综化学试卷(解析版) 题型:填空题
钴是人体必需的微量元素,含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用,请回答下列问题:
(1)Co基态原子的电子排布式为_____________;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到了广泛的应用,其结构如图所示,中心离子为钴离子。
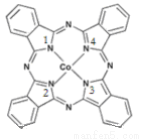
①酞菁钴中三种非金属原子的电负性有大到小的顺序为_____________,(用相应的元素符号作答);碳原子的杂化轨道类型为_____________;
②与钴离子通过配位键结合的氮原子的编号是_____________;
(3)CoCl2中结晶水数目不同呈现不同的颜色。
CoCl2·6H2O(粉红) 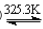 CoCl2·2H2O(紫红)
CoCl2·2H2O(紫红) CoCl2·H2O(蓝紫)
CoCl2·H2O(蓝紫)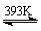 CoCl2(蓝色)
CoCl2(蓝色)
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用:_____________;
(4)用KCN处理含 Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3- ,写出该反应的离子方程式:_____________;
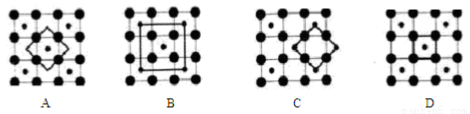
(5)Co的一种氧化物的晶胞如图所示( 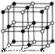 ),在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是_____________。
),在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是_____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前押题理综化学试卷(解析版) 题型:选择题
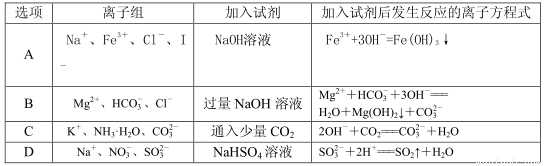
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下第四次月考化学试卷(解析版) 题型:选择题
4.6g铜镁合金完全溶解于100mL密度为1.40g/mL、质量分数为63%的浓硫酸中,得到4480mLNO2和336mLN2O4的混合气体(标准状况),向反应后的溶液中加入1.0mol•L-1NaOH溶液至离子恰好全部沉淀时,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是46:69
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C.产生沉淀8.51g
D.离子恰好完全沉淀时,加入NaOH溶液的体积是230mL
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下第二次月考化学试卷(解析版) 题型:填空题
铜(Cu)是一种重要的常见金属,现代电子器件的电路离不开它,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答下列问题:
(1) 向CuSO4溶液里逐滴加入氨水,首先生成蓝色难溶物,然后得到深蓝色溶液。由蓝色难溶物得到深蓝色溶液的离子方程式为__________________ ;写出该深蓝色离子能反映出特殊共价键的结构简式________________;
(2) 元素金(Au)处于周期表中的第六周期,与Cu同族。一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心、Au原子处于顶角位置,则该合金中Cu原子与Au原子数量之比为________;该晶体中,原子之间的作用力是________________________;
(3) 上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的最简化学式应为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:填空题
A、B、C、D 4种元素的核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层 电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。
电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。
请回答下列 问题:
问题:
(1)4种元素的符号依次是A________,B_________, C_________,D________。它们原子的半径由大到小的顺序是(要求写出化学符号)______________________________ ___。
___。
(2)C和D元素对应的最高 价氧化物对应水化物的碱性强弱顺序(要求写出化学式)__________。
价氧化物对应水化物的碱性强弱顺序(要求写出化学式)__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com