设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为22.4L
B.标准状况下,11.2L H2O 含有的分子数为0.5NA
C.常温常压下,32g O2和O3的混合气体所含原子数为2NA
D.1mol Fe和足量稀盐酸反应,铁失去的电子数为3 NA
【答案】
分析:A.N
A个氦原子的氦气物质的量是1mol;
B.H
2O在标准状况下不是气体;
C.利用n=
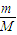
及O
2和O
3混合气体中分子都是只由氧原子构成来分析氧原子数;
D.Fe和足量稀盐酸反应生成二价铁.
解答:解:A.N
A个氦原子的氦气物质的量是1mol,在标准状况下的体积约为22.4L,故A正确;
B.标况下,水为液体,所以11.2L H
2O 在标准状况下物质的量不是1mol,故B错误;
C.因混合气体中分子都是只由氧原子构成,则氧原子的物质的量为
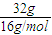
=2mol,氧原子数为2mol×N
A=2N
A,故C正确;
D.Fe和足量稀盐酸反应生成二价铁,1mol Fe和足量稀盐酸反应,铁失去的电子数为2N
A,故D错误.
故选BD.
点评:本题考查阿伏伽德罗常数的计算,难度不大,明确物质的状态、质量与物质的量的关系是解答的关键.

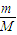 及O2和O3混合气体中分子都是只由氧原子构成来分析氧原子数;
及O2和O3混合气体中分子都是只由氧原子构成来分析氧原子数;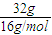 =2mol,氧原子数为2mol×NA=2NA,故C正确;
=2mol,氧原子数为2mol×NA=2NA,故C正确;

 备战中考寒假系列答案
备战中考寒假系列答案