
分析 向煤中加入石灰石作为脱硫剂,可以减少SO2的排放,生成CaSO4,
反应方程式为2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2CO2,根据关系式S~SO2~CaCO3~2CaSO4计算.
解答 解:向煤中加入石灰石作为脱硫剂,可以减少SO2的排放,生成CaSO4,
反应方程式为2CaCO3+O2+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2,
令需要加入x吨的石灰石,反应可得硫酸钙y吨,则:
S~SO2~CaCO3~CaSO4计算.
32 100 136
1t×1% x t y t
所以32:100=1t×1%:xt,解得x=0.03125,0.03125t=32.25kg
32:136=1t×1%:y t,解得y=0.0425,0.0425t=42.5kg
答:需要加入31.25千克的石灰石,反应可得硫酸钙42.5千克.
点评 本题考查根据方程式的计算,难度不大,书写方程式是关键,注意根据关系式计算的计算.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 遇氯化氢产生白烟 | B. | 能使湿润的蓝色石蕊试纸变红 | ||
| C. | 刺激性气味、密度比空气小 | D. | 其水溶液能使酚酞溶液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
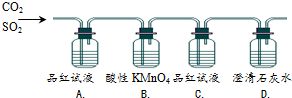
| 编号 | 实验现象 | 实验目的 |
| A. | 品红褪色 | 证明混合气体中有SO2 |
| B. | KMnO4褪色 | 证明SO2有还原性 |
| C. | 品红不褪色 | 证明进入C的气体中没有SO2 |
| D. | 石灰水变浑浊 | 证明混合气体中有CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医用消毒酒精是一种有机化合物 | |
| B. | 有沉淀生成的过程一定发生了化学变化 | |
| C. | 金属钠属于遇湿易燃危险化学品 | |
| D. | 泡沫灭火器中药剂为干冰和起泡剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化亚铁溶于稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | |
| B. | NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-=AlO2-+2H2O | |
| C. | Na2SiO3溶液与稀盐酸混合:Na2SiO3+2H+=2Na++H2SiO3↓ | |
| D. | Ca(HCO3)2溶液和Ca(OH)2溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molN2和1molCO所含的分子数都是NA | |
| B. | 1molH2和1molCO2所含的原子数都是NA | |
| C. | 1molCO和1molCO2所含的氧原子数都是NA | |
| D. | 1molH2SO4和1molH3PO4所含的原子数都是4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验内容 | 实验目的 |
| A | 分别将一小粒钠投入水与无水乙醇中,钠与水反应更剧烈 | 证明羟基氢活泼性: H2O>C2H5OH |
| B | 向滴有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液,溶液褪色 | 证明溴乙烷发生消去反应有乙烯生成 |
| D | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com