
【题目】对元素周期表和元素周期律的发现有突出贡献的科学家是
A. 拉瓦锡 B. 阿伏加德罗 C. 门捷列夫 D. 道尔顿
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 27g铝中加入lmol/L的NaOH溶液,转移电子数是3NA
B. 56gN2与CO混合物中原子总数是4NA
C. 标准状况下,44.8LNO与22.4LO2反应后的分子数是2NA
D. 常温下,lLpH=1的H2SO4溶液中的H+为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 25℃、101KPa条件下22克CO2所含的原子数目为1.5NA
B. 标准状况下0.1molH2O含有的分子数目为0.1NA
C. 0℃、101KPa条件下03NA氧气的体积是6.72升
D. 58.5克NaCl固体中含有的离子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中涉及的反应物和生成物共有4种物质:X、Cl2、NH3、N2。当转移的电子总数 a个时,氮气数量变化了b mol。
(1)氧化产物的摩尔质量是________________。
(2)阿伏加德罗常数为(用含a、b的代数式表示)______________。
(3)X可能有两种组成:HCl或NH4Cl,为确定X的化学式,某同学取同温同压下体积分别为V1、V2的两种物质(氧化剂与还原剂)充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温度后,再测出容器的容积(V3)。
①若实验结果(用V1、V2与V3间关系来表示,下同)是________________________,则X的化学式为HCl,简要写出你作出此推断的依据是_____________________。
②若实验结果是__________________,则X的化学式为NH4Cl。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.焓变是指1 mol物质参加反应时的能量变化
B.当反应放热时ΔH>0,反应吸热时ΔH<0
C.在加热条件下发生的反应均为吸热反应
D.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,ΔH为负值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是宝贵的自然资源,水的净化与污水处理是化学工作者需要研究的重要课题。
(1)在净水过程中用到混凝剂,其中不可以作为混凝剂使用的是__________。
A.硫酸铝 B.氧化铝 C.碱式氯化铝 D.氯化铁
(2)海水淡化是人类获得饮用水的一个重要方法,下列有关海水淡化处理的方法正确的是_____。
A.蒸馏法能耗最小,设备最简单;冷冻法要消耗大量能源
B.利用电渗析法淡化海水时,在阴极附近放阴离子交换膜,在阳极附近放阳离子交换膜
C.利用电渗析法淡化海水时,得到淡水的部分在中间区
D.利用反渗透技术可以大量、快速地生产淡水
(3)除了水资源,能源、信息、材料一起构成了现代文明的三大支柱。甲醇是一种重要的化工原料,以甲醇、氧气为基本反应物的新型燃料电池已经问世,其结构如图所示(甲醇解离产生的H+可以通过质子交换膜进入另一极)。请写出通入甲醇的电极上的电极反应式:____________。

某同学以甲醇燃料电池为电源,以石墨为电极电解500mL 0.2mol·L1 CuSO4溶液,则与电源正极相连的电解池电极上的电极反应式为:_______________________________;电解一段时间后,在电解池两极上共产生7.84 L气体(标准状况下),此时甲醇燃料电池中共消耗甲醇_________g 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中含有Mg2+、Ba2+ 、Ag+和NO3-,现分别用NaCl溶液、NaOH溶液和Na2CO3溶液将溶液中三种阳离子逐一完全沉淀分离,其流程如右图所示。下列说法正确的是( )

A. 试剂A可能为NaOH溶液
B. 沉淀2只能是BaCO3 ,不可能是Mg(OH)2
C. 每加一种试剂需过量但不需要过滤即可进行下一步
D. 生成沉淀1的离子方程式只能是:Ag+ + Cl- = AgCl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池以熔融金属Na、熔融S和多硫化钠[Na2Sx(3<x<5)]分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质。下列关于该电池的叙述错误的是( )
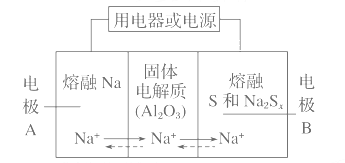
A. 放电时,电极B为正极
B. 充电时内电路中Na+的移动方向为从B到A
C. 该电池的工作适宜温度应该在Al2O3的熔点和沸点之间
D. 充电时阳极反应为S![]() -2e-===xS
-2e-===xS
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com