
| A�� | ԭ������������ѧ���ʻ��ã�����Ϊͬ�������� | |
| B�� | �������Ͻ�ı�Ĥ���ϻ�ѧ���ʻ��� | |
| C�� | ԭ�����������ķ��նԶ�������Ĥ��Ʒû��Ӱ�� | |
| D�� | ��������Ĥ��Ʒ���ʺ��������������� |
���� A��ͬ����������ͬ��Ԫ����ɵIJ�ͬ���ʣ�
B���������Ͻ�ı�Ĥ���ϣ�����ԭ�����������ķ����Ժ������仨���߱䰵��
C����Ʒ��¶��̫�ջ��������ø�Ϊ�ֲڣ�
D����������Ĥ��Ʒ����¶��̫�ջ��������ø�Ϊ�ֲڣ�
��� �⣺A��ͬ����������ͬ��Ԫ����ɵIJ�ͬ���ʣ�ԭ����������Ԫ�ص��ʣ���A����
B���������Ͻ��Dz����ý�������ѧ���ʽ��ȶ����������Ͻ�ı�Ĥ���ϣ�����ԭ�����������ķ����Ժ������仨���߱䰵����B����
C����Ʒ��¶��̫�ջ��������ø�Ϊ�ֲڣ�ԭ�����������ķ��նԶ�������Ĥ��Ʒ��Ӱ�죬��C����
D����������Ĥ��Ʒ����¶��̫�ջ��������ø�Ϊ�ֲڣ����ʺ�������������������D��ȷ��
��ѡD��
���� ���⿼���˻�ѧ��Ϣ�ķ����жϣ���Ҫ�ǺϽ�ͽ������ʵ�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��t/s | 0 | 50 | 150 | 250 | 350 |
| n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܶȴ�С����������ˮ���� | |
| B�� | �ۡ��е�ߵͣ��Ҵ������飾���� | |
| C�� | ��̼����С�����飾�Ҵ������� | |
| D�� | ������ȼ��ʱ�ĺ����������飾��ϩ����ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
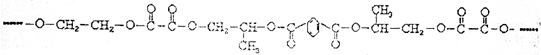



 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
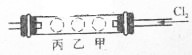 ��ͼ��ʾ����һ��Ӳ�ʲ��������˿�װ�д����ܵĵ����������Թ��е��ҡ��С���������λ���ֱ�������KI������Һ�ļ�����NaIŨ��Һ������ͽ���KBrŨ��Һ�ı���ʵ��ʱ�����Ҷ˻���ͨ��C12��ͬʱ���Ҵ����ȣ�������Դ��������������ƶ����۲쵽�������ǣ�
��ͼ��ʾ����һ��Ӳ�ʲ��������˿�װ�д����ܵĵ����������Թ��е��ҡ��С���������λ���ֱ�������KI������Һ�ļ�����NaIŨ��Һ������ͽ���KBrŨ��Һ�ı���ʵ��ʱ�����Ҷ˻���ͨ��C12��ͬʱ���Ҵ����ȣ�������Դ��������������ƶ����۲쵽�������ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | H-H | C-O | C=O | H-O | C-H |
| ���ܣ�KJ•mol-1�� | 436 | 326 | 803 | 464 | 414 |
| ��ͬʱ����CO2ת���� | T1 | T2 | T3 | T4 | T5 |
| ��Ӧ�� | 65% | 77% | 80% | 80% | 66.67% |
| ��Ӧ�� | 56% | 67% | 76% | 80% | 66.67% |
| ��Ӧ�� | 48% | 62% | 72% | 80% | 66.67% |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ��ʱ�����ڵ�ѹǿ��ԭ����0.8�� | |
| B�� | M��ƽ����Ӧ����Ϊ0.15 mol•L-1•min-1 | |
| C�� | x��ֵΪ1 | |
| D�� | ƽ��ʱP��Ũ��Ϊ0.25 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ʵ�����ô���ʯ�����ᷴӦ��ȡ������̼��CO32-+2H+�TCO2��+H2O | |
| C�� | ͭƬ������������Һ�У�Cu+Ag+�TCu2++Ag | |
| D�� | ��������ˮ�ķ�Ӧ��Na2O+H2O�T2Na++2OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com