
【题目】下列所有元素组合,既可以形成离子化合物,又可形成共价化合物的一组是
A.H、C、O、K B.H、N、O
C.H、O、S D.H、O、S、Na
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
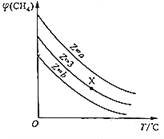
A. 该反应的焓变△H<0
B. 图中Z的大小为b<3<a
C. 图中X点对应的平衡混合物中![]() =3
=3
D. 温度不变时,图中X点对应的平衡在加压后![]() (CH4)增大
(CH4)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 食用白糖的主要成分是蔗糖 B. 淀粉、纤维素和油脂都是属于天然高分子化合物
C. 植物油的主要成分是高级脂肪酸 D. 蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中充入一定量的NO2,发生反应2NO2(g)![]() N2O4(g)△H=﹣57kJmol﹣1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化
N2O4(g)△H=﹣57kJmol﹣1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化
的曲线如图所示。下列说法正确的是( )
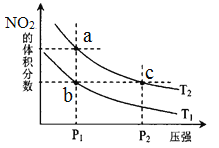
A. a、c两点的反应速率:a>c
B. a、b两点的转化率:a<b
C. a、c两点气体的颜色:a深,c浅
D. 由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
Ⅰ.氮氧化物的研究
(1)一定条件下,将2mol NO与2mol O2置于恒容密闭容器中发生反应:2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
A.混合气体的密度保持不变
B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变
D.O2的消耗速率和NO2的消耗速率相等
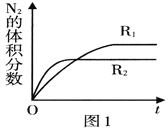
(2)已知反应. 2NO(g) ![]() N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
A.压强 B.温度 C.催化剂
根据图2中的能量变化数据.计算反应2NO(g) ![]() N2(g)+O2(g)的ΔH=__________
N2(g)+O2(g)的ΔH=__________

Ⅱ.碳氧化物研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
①T1_____ T2(填“>”或“<”或“=”),理由是____________________。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_________,该温度下的化学平衡常数为________ 。
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(图3乙)中,在T2℃下达到平衡,此时反应的平衡常数为_________;若再向容器中通入l mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量_________(填“变大”或“变小”或“不变”)。
(4)一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将a mol的CO通入2 L bmol/L NaOH 溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液(假设溶液体积不变),测得溶液中c(Na+)=c(HCOO-),则该混合溶液中甲酸的电离平衡常数 Ka=____________ (用含a和b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是关于反应A2(g)+3B2(g)2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
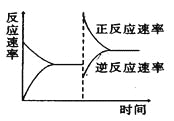
A. 升高温度,同时加压 B. 降低温度,同时减压
C. 增大反应物浓度,同时减小生成物浓度 D. 增大反应物浓度,同时使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. O2与O3互为同素异形体
B. 35Cl与37Cl互为同位素,两者核外电子排布不同
C. CH4与C3H8一定互为同系物
D. CH3CH2NO2与H2NCH2COOH互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com