
【题目】三氧化二镍是一种重要的电子元件材料、蓄电池材料。工业上利用含镍废料(以镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
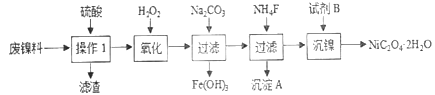
(1)操作1的名称为__________。
(2)保持其他条件相同,在不同温度下对废镍料进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为_______(填字母)。
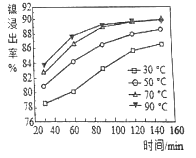
a.30℃、30min b.70℃、120min
c.90℃、150min d.90℃、120min
(3)沉淀A为CaF2和_________(填化学式)。
(4)试剂B的化学式为_________________。
(5)NiC2O4·2H2O样品经某稀酸酸化处理后,用稀KMnO4标准溶液滴定[在本实验条件下,Ni(Ⅱ)不能被氧化,其他物质不参与反应],通过测定草酸的量可测定NiC2O4·2H2O样品的纯度,滴定反应为:2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O。实验中称取0.183g样品,滴定时消耗了0.0400mol.L-1的KMnO4溶液8.00mL,则该样品中NiC2O4·2H2O的质量分数为_________。
(6)高温煅烧草酸镍制取三氧化二镍时会产生CO、CO2、水蒸气等混合气体。某同学设计如下实验流程进行检验。
混合气体![]() 现象
现象![]() 现象
现象![]()
![]() 现象
现象![]() 现象
现象
①试剂1的名称为____________。
②证明混合气体有CO的现象是_____________________________________________。
【答案】 过滤 b MgF2 H2C2O4或Na2C2O4(或可溶性的草酸盐等) 80.0% (无水)硫酸铜 黑色氧化铜(试剂2)变红色,澄清石灰水(试剂3)变浑浊(答案合理即可)
【解析】(1)镍废料中的镍、铁、钙、镁均可以和硫酸反应没生成硫酸盐,且硫酸钙属于微溶物,经过过滤除去不反应的杂质,和硫酸钙的不溶物,故操作1为过滤。
(2)根据图中的数据,在30℃、30 min时,镍的浸出率只有不到80%,此浸出率太低;在90℃时,120 min和150 min时的浸出率接近;而在120 min时,70℃和90℃时的浸出率相同。考虑经济效益还是选择低温合算,故选b。
由图知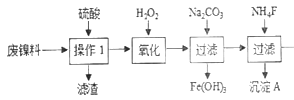 操作1除去了不溶的硫酸钙双氧水氧化Fe2+为Fe3+,加碳酸钠调节PH使Fe3+沉淀出来,加氟化铵,产生的沉淀为CaF2和MgF2。答案:MgF2。
操作1除去了不溶的硫酸钙双氧水氧化Fe2+为Fe3+,加碳酸钠调节PH使Fe3+沉淀出来,加氟化铵,产生的沉淀为CaF2和MgF2。答案:MgF2。
经过上述处理,除去铁、钙、镁等杂质,由图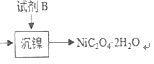 知试剂B为H2C2O4或Na2C2O4(或可溶性的草酸盐等)答案:H2C2O4或Na2C2O4(或可溶性的草酸盐等)
知试剂B为H2C2O4或Na2C2O4(或可溶性的草酸盐等)答案:H2C2O4或Na2C2O4(或可溶性的草酸盐等)
(5)根据反应方程式为:2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O 根据反应关系
5NiC2O4·2H2O---- 5H2C2O4-----2 MnO4-
X 0.0400mol.L-1![]() 8.00mL/1000
8.00mL/1000
X=8![]() 10-4mol
10-4mol
样品中NiC2O4·2H2O的质量分数为=8![]() 10-4mol
10-4mol![]() 183g/moL/0.183g=80.0%
183g/moL/0.183g=80.0%
(6) ① 高温煅烧NiC2O4的产物为三氧化二镍.CO、CO2、水蒸气,检验生成物时应先检验水,所以试剂1为无水硫酸铜.答案: 硫酸铜 。
②证明混合气体有CO的现象是
混合气体![]() 现象
现象![]() 现象
现象![]()
![]() 现象
现象![]() 现象
现象
根据上图知试剂1为硫酸铜,鉴别水,澄清的石灰水,鉴别CO2,试剂2为检验CO,可用黑色氧化铜粉末变红,再用澄清石灰水(试剂3)变浑浊即可。答案 :黑色氧化铜(试剂2)变红色。澄清石灰水(试剂3)变浑浊


科目:高中化学 来源: 题型:
【题目】为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是
A. Na2O2中阴、阳离子的个数比为1∶1
B. Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C. Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D. Na2O2漂白后的有色物质受热后能恢复原色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KC1O3和草酸(H2C2O4)在60℃时反应制得。某学生用下图所示的装置模拟工业制取及收集C1O2,其中A为C1O2的发生装置,B为C1O2的凝集装置,C为尾气吸收装置。
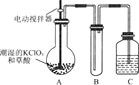
请回答下列问题:
(1)A中反应产物有K2CO3、C1O2和CO2等,请写出该反应的化学方程式:________________________。
A部分还应添加温水浴控制温度在60 °C,B部分还应补充什么装置:_________________。
(2)该装置按(1)补充完整后,装置A、B、C中还有一处设计明显不合理的是_____(填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),该反应的离子方程式为____________。若实验时需要450 mL 4 mol L-1的NaOH溶液,则在精确配制时,需要称取NaOH的质量是____g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
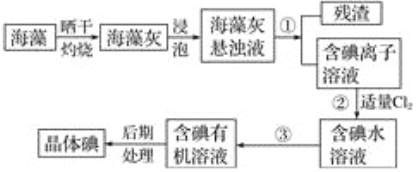
(1)实验室焙烧海带,需要下列仪器中的________(填字母)。
a.试管 b.烧杯c.坩埚 d.泥三角e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①________,③________。
(3)提取碘的过程中,可选择的有机试剂是________(填字母)。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有________、________。
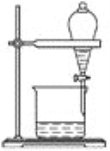
(5)小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈________色;他们打开分液漏斗活塞,却未见液体流下,原因可能是_________________________________________。
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
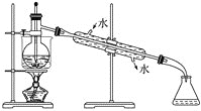
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
(7)进行上述蒸馏操作时,使用水浴加热的原因是________________________________________________,最后晶态碘在________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列物质分类全部正确的是( )
①苏打 ②食盐水 ③石灰水 ④NaOH ⑤液氧 ⑥KClO3
A.纯净物—③④⑤B.混合物—②⑤
C.盐—①⑥D.碱—①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出),单质A常作为食品包装材料,甲是两性氧化物。
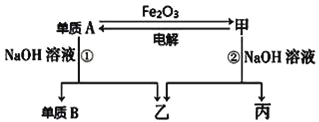
根据图示转化关系回答:
(1)写出反应①的离子方程式:_________________。
(2)实验室完成单质A与Fe2O3反应实验,需要的试剂还有_______。
a.KCl b.KClO 3 c.MnO2 d.Mg
(3)利用该反应的原理,工业上可用于___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内含量虽然很少,却是维持正常生命活动不可缺少的。这可通过下面的哪一实例得到证实( )
A.缺Mg时叶片变黄
B.油菜缺B时只开花不结果
C.动物血液中钙盐的含量太低会抽搐
D.缺P会导致作物植株矮小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com