
����Ŀ��A��B��C��D��E��F����Ԫ�ص�ԭ��������������A����ۺ���ͼ۵ľ���ֵ��ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ��δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�F�Ļ�̬ԭ�ӵ�3d�����4s��������4������ش��������⣺
��1��F�Ļ�̬ԭ�˼۵����Ų�ʽΪ��
��2��B��C��D��E��ԭ�ӵĵ�һ��������С�����˳��Ϊ������Ԫ�ط��Żش�
��3�����й���B2A2���Ӻ�A2D2���ӵ�˵����ȷ������
A.�����ж����ЦҼ��ͦм�
B.����ԭ�Ӷ�sp�ӻ�
C.���Ǻ����Լ��ͷǼ��Լ��ķǼ��Է���
D.��Ϊ�ȵ�����
E.B2A2���ӵķе����Ե���A2D2����
��4��F2+����BD�����γ�[F��BD��4]2+ �� ��ԭ����BD�����к�����
��5����B��E��F����Ԫ���γɵ�һ�־��г����Եľ��壬������ͼ��ʾ��Bλ��E��Fԭ�ӽ��ܶѻ����γɵĿ�϶���У���һ��Fԭ�Ӿ��������Fԭ�ӵ���ĿΪ �� �þ���Ļ�ѧʽΪ �� ���þ������Է�������ΪM�������ӵ�����ΪNA �� B��E��F����Ԫ�ص�ԭ�Ӱ뾶�ֱ�Ϊr1pm��r2pm��r3pm����þ�����ܶȱ���ʽΪ �� 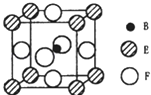
���𰸡�
��1��3d84s2
��2��Mg��C��O��N
��3��E
��4���µ��Ӷ�
��5��8��MgNi3C��![]()
��������A��B��C��D��E��F����Ԫ�ص�ԭ������������������B�Ļ�̬ԭ����3����ͬ���ܼ����Ҹ��ܼ��еĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p2 �� ��BΪ̼Ԫ�أ�A��������ۺ�����۵ľ���ֵ��ȣ�ԭ����������̼����AΪHԪ�أ�E�Ļ�̬ԭ�ӵ�s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p4��1s22s22p63s2 �� D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��D��ԭ������С��E��ԭ�Ӻ�������Ų�ֻ��Ϊ1s22s22p4 �� ��DΪOԪ�أ���EΪMg����C��ԭ����������̼����֮�䣬��CΪNԪ�أ�F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����4s����ֻ����2�����Ӳ㣬��ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d84s2 �� ��FΪNi����1��F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����4s����ֻ����2�����Ӳ㣬3d�ܼ���8�����ӣ���ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d84s2 �� �۵����Ų�Ϊ3d84s2 ��
���Դ��ǣ�3d84s2����2��C��N��O��Mg����Ԫ�أ�Mg���ڽ�������һ��������С��C��N��Oͬ���ڣ���ԭ����������ĵ�һ�����ܳ��������ƣ���NԪ��2p�ܼ�����3�����ӣ����ڰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ��������С�����˳��ΪMg��C��O��N�����Դ��ǣ�Mg��C��O��N����3��A��C2H2�����к���C��C������C��H�������ЦҼ��ͦм�����H2O2����ΪH��O��O��H��ֻ���ЦҼ�����A����B��C2H2������Cԭ�ӳ�2���Ҽ���û�й¶Ե��ӣ��ӻ������ĿΪ2����ȡsp�ӻ���H2O2������Oԭ�ӳ�2���Ҽ�������2�Թµ��Ӷԣ��ӻ������ĿΪ4����ȡsp3�ӻ�����B����C��C2H2��ֱ���ͶԳƽṹ���ǷǼ��Է��ӣ���H2O2������չ����ҳ�νṹ�����ڼ��Է��ӣ���C����D��C2H2���ӡ�H2O2���Ӻ��е���������۵�����������ȣ����ǵȵ����壬��D����E��C2H2������Ϊ��̬����H2O2������ΪҺ̬����E��ȷ�����Դ��ǣ�E����4��Ni2+����CO����ͨ����λ���γ�[Ni��CO��4]2+ �� ��ԭ����CO�����к��йµ��Ӷԣ����Դ��ǣ��µ��Ӷԣ���5�����ϵ�������Fԭ���о�����֮���������Fԭ��λ�ھ����������漰ǰ���������ϣ��������ϵ���Ϊ�ϲ㾧�����µ��棬����֮�����Fԭ����8����
�ɾ���������֪��������Cԭ����Ŀ=1��NiԪ����Ŀ=6�� ![]() =3��Mgԭ����Ŀ=8��
=3��Mgԭ����Ŀ=8�� ![]() =1���ʸþ���Ļ�ѧʽΪMgNi3C����������=
=1���ʸþ���Ļ�ѧʽΪMgNi3C����������= ![]() g���ϵ���Խ��߳���=��2r2+2r3��pm=��2r2+2r3����10��10cm���ʾ����ⳤ=
g���ϵ���Խ��߳���=��2r2+2r3��pm=��2r2+2r3����10��10cm���ʾ����ⳤ= ![]() ����2r2+2r3����10��10cm=
����2r2+2r3����10��10cm= ![]() ��r2+r3����10��10cm���������=[
��r2+r3����10��10cm���������=[ ![]() ��r2+r3����10��10cm]3=2
��r2+r3����10��10cm]3=2 ![]() ��r2+r3��3��10��30cm3 �� �ʾ����ܶ�=
��r2+r3��3��10��30cm3 �� �ʾ����ܶ�= 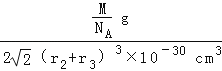 =
= 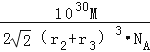 g��cm��3 �� ���Դ��ǣ�8��MgNi3C��
g��cm��3 �� ���Դ��ǣ�8��MgNi3C��  ��
��


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С��������������������pH��Χ��6.3��7.5�����п����ڲⶨ������ҺpH�Ҿ�ȷ����ߵ��ǣ�������
A.���ָʾ��
B.pH��
C.����pH��ֽ
D.�㷺pH��ֽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X�����������X2O 4.7g����95.3gˮ�У��õ�������������Ϊ5.6%����Һ��Y��Xλ��ͬһ�壬12g Y������������400mL 0.75molL ��1��������ȫ�кͣ�Z��Yͬ���ڣ���״����5.6L ZO2Ϊ16g��
��1����X��Y��Z�����ԭ��������
��2��д����Ԫ�ط��ţ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������CO2����ͨ��NaOH��Ca��OH��2��NaAlO2�Ļ����Һ�С���֪NaAlO2��CO2��Ӧ����Al��OH��3���������ɳ��������ʵ�����ͨ��CO2������Ĺ�ϵ�ɱ�ʾΪ��������
A.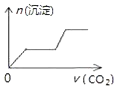
B.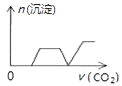
C.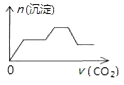
D.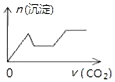
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������70�����ı�����ϣ�ʳƷ�������ڿ����γɵ�����ʴ�����������̵�ӡ������õ�徫��ż�졢�μ��������ơ�̪�����ȶ��dz��õĺ���Һ���ɫ���̼�������Ϊ���ǣ� ��
A.�ױ�����B.�ױ���ԭC.�ֽ�D.�ӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����������������
A. ���ڿ�����ȼ�գ���������ɫ����
B. ��������̼ͨ��ˮ�У�����������
C. ������ͭ˿�ھƾ��ƻ��������գ�ͭ˿������
D. һ����̼ͨ�����ȵ�����������ɫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ���������л��е����ʣ���ѡ�õ��Լ���������������ȷ����
���� | ���� | ������Ӧѡ�õ��Լ��Ͳ������� | |
A | CO2 | CO | ͨ��O2����ȼ |
B | NaOH���� | Na2CO3���� | ����������ᣬ���� |
C | Cu(NO3)2��Һ | AgNO3��Һ | ���������ͭ�ۣ����� |
D | KNO3��Һ | KOH��Һ | ����������CuSO4��Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��BF3��һ������ˮ�γɾ���Q[��H2O��2BF3]��Q��һ�������¿�ת��ΪR�� 
��1������Q�и�����������������漰������ĸ����
a�����Ӽ� b�����ۼ� c����λ��
d�������� e����� f�����»���
��2��R�������ӵĿռ乹��Ϊ �� �����ӵ�����ԭ�ӹ�������ӻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����칤���������������(��)���졢�Ʒ����Գ�һ�ֶ��ɣ��仯���������˼���������¯����ǽ�����侲֮ʱ����ǽ����Ȼ��������������ȡ��������Ի�Ʒ����������������ָ
A.FeSO4��7H2OB.ZnSO4��7H2OC.Fe2(SO4)3��9H2OD.Fe2O3��nH2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com