
| 分子 | 立体结构 | 杂化方式 | |
| A | 三氧化硫(SO3) | 正三角形 | S原子采用sp杂化 |
| B | 二氧化硫(SO2) | V型 | S原子采用sp3杂化 |
| C | 碳酸根离子(CO32-) | 三角锥型 | C原子采用sp2杂化 |
| D | 乙炔(C2H2) | 直线型 | C原子采用sp杂化 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据价电子对互斥理论确定微粒的空间构型和原子的杂化方式,价层电子对个数=σ键个数+孤电子对个数.
解答 解:A.SO3 分子中价层电子对个数=σ键个数+孤电子对个数=3+$\frac{1}{2}$(6-3×2)=3,所以硫原子采用sp2杂化,为平面三角形结构,故A错误;
B.SO2的价层电子对个数=2+$\frac{1}{2}$(6-2×2)=3,硫原子采取SP2杂化,该分子为V形结构,故B错误;
C.碳酸根离子中价层电子对个数=σ键个数+孤电子对个数=3+$\frac{1}{2}$(4+2-3×2)=3,所以原子杂化方式是sp2,为平面三角形结构,故C错误;
D.乙炔(CH≡CH)分子中每个C原子含有2个σ键和2个π键,价层电子对个数是2,为sp杂化,为直线型,故D正确;
故选D.
点评 本题考查了原子杂化方式的判断和微粒的空间构型的判断,根据价层电子对互斥理论来分析解答即可,注意孤电子对个数的计算方法,为易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题
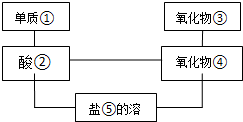 给图中①~⑤选择适当的物质,使有连线的两物质能发生反应.供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉.
给图中①~⑤选择适当的物质,使有连线的两物质能发生反应.供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上将NH3与CO2在高温高压下制成[CO(NH2)2] | |
| B. | 空气中的O2和N2在闪电时化合成NO | |
| C. | 豆科植物的根瘤菌把氮气变为NH3 | |
| D. | 工业上用N2和H2来合成NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
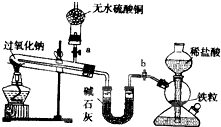 Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用双缩脲试剂可区分蛋白质溶液和淀粉溶液 | |
| B. | 用水可区分苯,甲苯和溴苯 | |
| C. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| D. | 用溴水可鉴别苯酚溶液,2-己烯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的结构式:H-O-O-H | B. | C2H4的结构简式:CH2CH2 | ||
| C. | O2-结构示意图: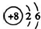 | D. | CCl4的结构式: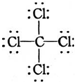 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
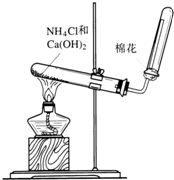 如图是实验室制取氨气的装置图.请回答:
如图是实验室制取氨气的装置图.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com